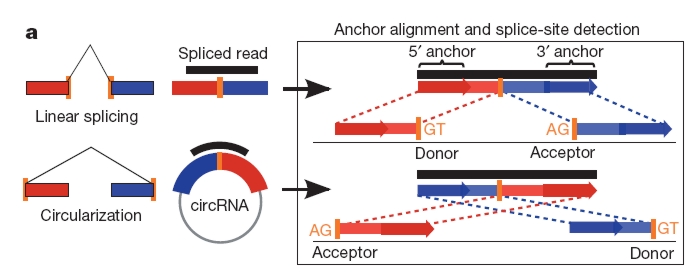
 Korábban a GENERA adatbázis kapcsán már pedzegettük, hogy mennyi közlemény létezik, amelyek génmódosított szervezetek hatásaival foglalkoznak, de nemrég megjelent egy rövidke összefoglaló a kérdésről, úgyhogy újra visszatérnék rá.
Korábban a GENERA adatbázis kapcsán már pedzegettük, hogy mennyi közlemény létezik, amelyek génmódosított szervezetek hatásaival foglalkoznak, de nemrég megjelent egy rövidke összefoglaló a kérdésről, úgyhogy újra visszatérnék rá.
A szerző nem lacafacázott, végigböngészte a teljes szakirodalmat 1994 -től napjainkig és kiválogatta azokat a közleményeket, amelyek elsődleges közlemények, referált folyóiratokból, kísérleti eredményeket közölnek és a génmódosított élőlények hatásaival foglalkoznak. Ebből a gyűjteményből így kimaradtak az összefoglaló közlemények, a vélemények, válaszok a szerkesztőknek, stb. vagyis minden ahol nem kísérletesen vizsgálták a GMOk hatásait. Így a bármilyen módon génmódosított élőlényekkel foglalkozó >32000 közleményből összesen 698 ment át a szűrőn, ez is szédületesen nagy szám (akinek kedve támad, végignézheti egyesével is a közleményeket). Nem meglepő módon ezen közlemények kevesebb, mint 5% -ában véltek látni bármilyen negatív hatást.
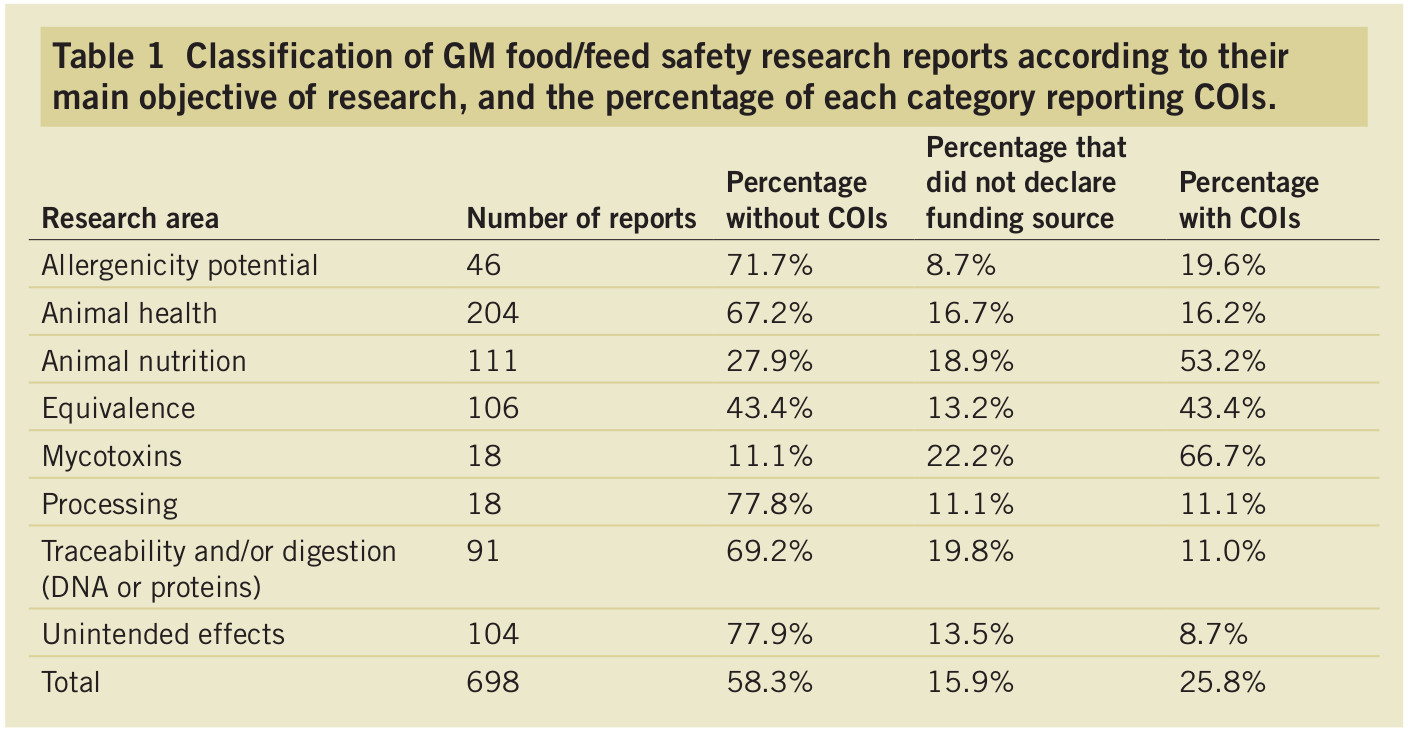
Ezek után arra volt kíváncsi a szerző, hogy ezeknek a közleményeknek mekkora hányadában található valamilyen “conflict of interest (COI)”, vagyis olyan körülmény, amely esetleg elhomályosíthatja a tisztánlátását, például ha a vizsgálatokat végző kutató mellékállásban a Monsanto alkalmazottja, vagy a laborja teljes költségvetését a Biotermesztők Szövetsége állja. Az eredmény látható a táblázatban, az első oszlop a témakör, a második az erről megjelent közlemények száma, a harmadik a COI nélküli közlemények aránya ezek közül, a negyedik azon közleményeknek az aránya, amelyeket független kutatók végeztek ugyan, de nem nyilatkoztak arról, ki pénzelte a kutatást, az utolsó oszlop pedig a COI -val rendelkező közlemények arányát mutatja. Az eredmény nem meglepő, a GMO -kat bevizsgáló közlemények több mint fele teljesen független kutatók munkája, alig negyede esetében áll csak fönn valamilyen függő viszony, nyilván ebből nem lehet tudni, hogy milyen irányban, valakinek az is elhomályosíthatja az éleslátását, ha biotermékeket vásárol.
Magyarul a GMOk biztonsága egy messze túlkutatott terület, a vizsgálatokat nagyrészt független műhelyekben végezték, egészen egyértelmű eredménnyel: Biztonságosak.
Sanchez, M.A., 2015. Conflict of interests and evidence base for GM crops food/feed safety research. Nat Biotech 33, 135–137. doi:10.1038/nbt.3133

 A gerincesek
A gerincesek  Azt hiszem az senkinek nem mond újat, hogy a kevés alvás negatív hatással van a szervezetre. Azon kívül, hogy a koncentrációs készség és az éberség csökken, a hosszú távú kialvatlanságnak komoly fiziológiai következményei is lehetnek; nagyobb eséllyel alakul ki elhízás, cukorbetegség, szív- és érrendszeri megbetegedés, és úgy átlagban nő a halálozási arány a krónikusan keveset alvók között – márpedig a CDC szerint az amerikaiak nagy többsége rendszeresen napi 6 óránál kevesebb alszik, ami már kimeríti a fenti kategóriát [1].
Azt hiszem az senkinek nem mond újat, hogy a kevés alvás negatív hatással van a szervezetre. Azon kívül, hogy a koncentrációs készség és az éberség csökken, a hosszú távú kialvatlanságnak komoly fiziológiai következményei is lehetnek; nagyobb eséllyel alakul ki elhízás, cukorbetegség, szív- és érrendszeri megbetegedés, és úgy átlagban nő a halálozási arány a krónikusan keveset alvók között – márpedig a CDC szerint az amerikaiak nagy többsége rendszeresen napi 6 óránál kevesebb alszik, ami már kimeríti a fenti kategóriát [1]. Egy felnőtt ember normál testi sejtje csak meghatározott számú osztódásra képes. A kromoszómavégeken a DNS másolását végző enzimrendszer ugyanis nem képes hatékonyan működni (a jelenség hátteréről bővebben
Egy felnőtt ember normál testi sejtje csak meghatározott számú osztódásra képes. A kromoszómavégeken a DNS másolását végző enzimrendszer ugyanis nem képes hatékonyan működni (a jelenség hátteréről bővebben