
Újságírói/ismeretterjesztői szempontból hálás téma, mert klikk-barát, ugyanakkor tudományos értékét erősen mérsékeli az aránytalan PR-hype, mi az? Egy újabb hír a mamutklónozásról…
Egy kattintás ide a folytatáshoz….

Újságírói/ismeretterjesztői szempontból hálás téma, mert klikk-barát, ugyanakkor tudományos értékét erősen mérsékeli az aránytalan PR-hype, mi az? Egy újabb hír a mamutklónozásról…
Egy kattintás ide a folytatáshoz….Mivel a blog tetszhalálán minden évben szeretnénk változtatni, de végül nem tudunk, így maradjon az eseti posztolás, főleg olyan anyagokkal, amelyek máshol jelentek meg.
Az egyik legrégebben futó posztsorozatunk a “Miért jó a GMO?”, amiben főleg Sexcomb kolléga vetette gépbe a témáról szóló gondolatait. Talán ehhez csatlakoztatható a legjobban a Qubitnek pár hete adott interjúm, amiben ugyan a GMO is terítékre kerül, de inkább általánosabban a géntechnológia volt terítéken.
Akit pedig esetleg ugyanennek a témának a kicsit “bulvárosabb” feldolgozása érdekel, annak ajánlom a radiocafé “Kávézó a világ végén” c. műsorában megejtett beszélgetést:
Egy sci-fi számára talán az a legnagyobb elismerés, amikor nem a valóság inspirálja a történetet, hanem a fikció a valóságot. Ebből a szempontból egész biztos, hogy az 1993-as Jurassic Park minden valós és vélt hibájával együtt fontos referenciaponttá vált. Jól lemérhető ez azon is, hogy amint képesek lettünk olyan, a film bemutatásakor még teljesen fikciós kategóriába eső dolgokra, mint az ősi, ma ma már nem élő fajok örökítőanyagának leolvasása, illetve szinte tetszőleges állati genom célzott manipulálása, szinte nincs olyan témába vágó interjú, amiben Steven Spielberg mára klasszikussá vált filmje elő ne kerülne. Ráadásul a témába vágó interjúknak gyakran az adja az apropóját, hogy a fent említett újítások nyomán valóban elindultak olyan programok, amelyek konkrétan kihalt fajok feltámasztását (vagy valami hasonlót) tűzték zászlajukra. Igaz, a mamut vagy a vándorgalamb esetében földtörténeti mértékkel mérve nemrég kihalt fajokról van szó, amelyeknek közeli rokonfajai ma is élnek, de ez általában vagy elveszik a beszélgetésekben, vagy egy logikus korai lépésként tűnik fel a dinoszauruszok „feltámasztásának” útján.
Ilyen szempontból talán nem is annyira meglepő a Tesla és a SpaceX alapítója, Elon Musk egyik munkatársának, Max Hodaknak minapi kinyilatkozása, miszerint egy kis odafigyeléssel és kellő erőforrások befektetésével 15 év alatt valamilyen formában megvalósíthatnánk a Jurassic Park vízióját, és „szuperegzotikus új fajokat” hozhatnánk létre.
A valóság sajnos az, hogy ennek nincs túl sok valóságalapja, és hacsak nem növekedési hormonnal telenyomott aligátorokban gondolkozunk, akkor 15 év alatt körülbelül annyira lehetne hitelesen rekreálni a Jurassic Park akár csak 1-2 lakóját is, mint amennyire hitelesen helyettesíti a szegény ember állatkertjében a tibeti masztiff az oroszlánt.
Kezdjük a rossz hírrel: a dinoszauruszok feltámasztásának a filmben látott módja (borostyánba zárt szúnyogból szekvenált DNS-darabokat „keverünk” kétéltű-genomokba) biztos nem fog működni, hiszen azóta bebizonyosodott, hogy a nukleinsavak egyszerűen nem elég stabilak ahhoz, hogy sok tízmillió éven át ellenálljanak az idő vasfogának. A használható DNS-darabok fennmaradásának rekordja most úgy 1 millió év körül van, de ez is különösen optimális körülmények között megőrzött mamutmaradványokból származik, és már nagyon-nagyon töredékes. Annak az esélye, hogy 60+ millió éves DNS-t találjunk értelmezhető mennyiségben, praktikusan nulla.
De nemhogy használható DNS-t nem tudtunk eddig izolálni, hanem még a sokkal stabilabb és csontokban nagy mennyiségben megtalálható fehérje, a kollagén korábban feltételezett jelenlétét sem sikerült minden kétséget kizáróan igazolni. Így tulajdonképpen mindennemű szekvenciaadat nélkül kell(ene) elkezdenünk a dinoszauruszok rekonstruálását. Vagyis, ellentétben a mamutok és vándorgalambok deextinkcióját megcélzó programokkal itt még arról sincs szó, hogy a korábban kihalt faj genomjának ismeretében próbáljuk egy ma élő, közeli rokon faj genomját átalakítani a fontosnak tűnő mutációk bevitelével. Nincs titkos ősi recept, amit felhasználhatunk dinoszauruszok építéséhez – azt újból ki kellene találni.
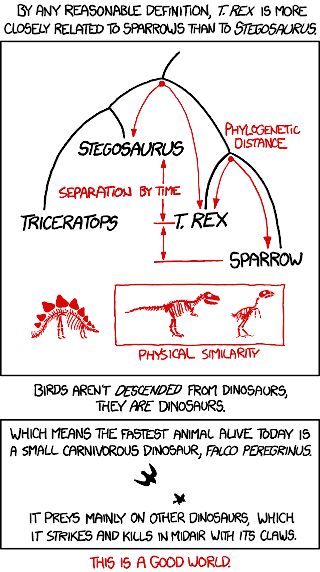
Az elmúlt közel három évtized fontos fejleménye viszont, hogy most már nem igazán kérdéses: a Jurassic Park talán legikonikusabb szereplőinek tartott „raptorok” ma is élő legközelebbi rokonai madarak. Ezt az utóbbi évtizedek paleontológiai anyaga, különösen a kínai lelőhelyeken nagy számban feltárt „tollas dinók” eléggé egyértelművé tették, és nem mellesleg ezeknek a leleteknek is köszönhetően nagyot változott az, hogy miképp képzeljük el ezeket az egykor élt óriáshüllőket – a pikkelyes bőrt fokozatosan felváltotta a tollas kinézet.
Így aztán praktikusabb, ha mondjuk egy ősi madárcsoport valamelyik egyedéből indulunk ki. Ha már elég nagy és egy kicsit vad is, az jó kiindulás lehet, így képzeletünket elengedve, válasszuk mondjuk az egyébként is gyakran a bolygó legveszélyesebb madarának nevezett és lábai miatt rendszeresen a dinoszauruszokhoz hasonlított kazuárt.
Mivel van olyan kazuárfaj, aminek a genomja ismert, ez nem teljesen elvetemült ötlet, nincs ismert fizikai akadálya, hogy legalább is megpróbáljuk szerkeszteni. Ha egy mai kazuárt egy korabeli (méretben összevethető) Deinonychus-hoz hasonlítunk, így is szembetűnik pár lényeges külalakbeli különbség, amelyeken változtatni kellene. Ilyen például, hogy a kazuároknak fogatlan csőrük van, mellső végtagjukon nincsenek karmok, illetve igen látványos a hosszú posztanális farok hiánya. Ezek orvoslása lenne az a minimum, amire szükségünk lenne, hogy a kölalakot tekintve valóban valami raptorszerű, „szuperegzotikus új fajt” hozzunk létre.
Egyik területen sincs könnyű dolgunk, de talán annak a megoldása lenne a legegyszerűbb, hogy a mellső végtagokon is karmok legyenek. Ilyen madarat ugyanis ismerünk: ez a dél-amerikai esőerdők lakója, a hoacin, amelynek fiatal egyedei mindkét szárnyukon két-két jól fejlett karommal rendelkeznek, amelyeket a mászáshoz tudnak használni. Igaz, ezek a karmok az idősebb állatokban eltűnnek, de mégis, puszta jelenlétük azt sugallja, hogy nem lenne lehetetlen előhozni egy madárgenomból a karmos mellső végtagokat. Bónusz pont, hogy a hoacin genomját is ismerjük – igaz, egyelőre nem tudjuk, hol keressük benne a karmos szárnyak megjelenéséhez szükséges genetikai információt, de mégis van miből kiindulnunk, és jó közelítéssel (legyünk optimisták és megengedőek) olyan 5-10 év alatt egy kellően ambiciózus projektben sikerülhet ezt a jelleget feltérképezni és esetleg más madarakban is létrehozni.

Ennél lényegesen nagyobb falat lenne a csőr visszaállítása fogas szájjá. A csőr evolúciója két lépésben következett be: a fosszíliák tanúsága szerint előbb az állkapocs vett fel jellegzetes csőrformát, és ezt követte a fogak elvesztése. Részben ez támasztja alá, hogy az egyik legklasszikusabb és híresebb csirkemutáns, a talpid egyik eredménye, hogy a fejlődő csőrökben megjelennek a fogak. Igaz, a mutáció számos más fenotípusos következménnyel jár, amelyek összességében ahhoz vezetnek, hogy a homozigóta talpid mutánsok nem életképesek, de legalább van valami kiindulópontunk.
Hasonlóan arról is tudunk egy keveset, hogy mi kellene ahhoz, hogy egy csirkecsőrt ismét állkapocsszerűvé tegyünk: bő fél évtizeddel ezelőtt már sikerült úgy manipulálni fejlődő csirkék állkapcsát, hogy az lényegesen szélesebb lett, már-már raptorállkapocs-szerű. A dolog szépségét rontja némileg, hogy mindezt csak egyes jelátviteli útvonalak átmeneti bekapcsolásával érték el és nem a genom szerkesztésével, de ha ismét kellően optimisták vagyunk, mondhatjuk azt, hogy 10-15 év alatt megfejtjük, hogyan lehetne genetikai változások segítségével létrehozni egy dinoszauruszszerű szájat.
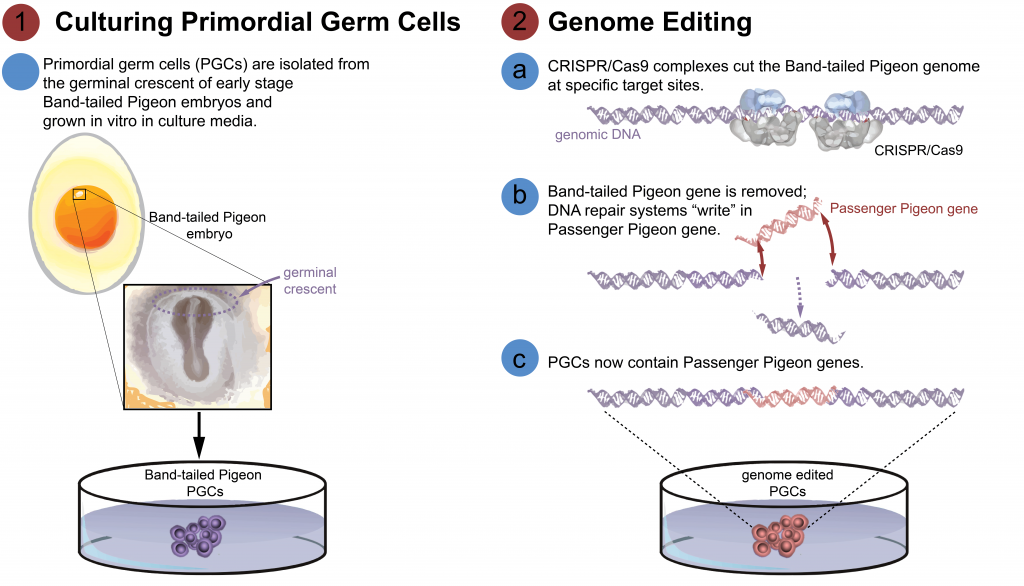
Ez volt persze a dolgok könnyebbik fele, és még ennek a két jellegnek a kazuárgenomba való bevitelét is meg kellene oldani, ami szintén nem ígérkezik sétagaloppnak, mivel a madarak genomszerkesztése kifejezetten kemény dió. Egy emlős-, kétéltű- vagy halembriótól eltérően egy megtermékenyített madár-petesejtet nem tudunk petricsészében létrehozni és génszerkeszteni, majd megnézni, mi lesz ennek az eredménye (halakban és kétéltűekben a fejlődés eleve külső, az emlősökben a megtermékenyített embriót vissza lehet ültetni a méhbe). Ezért is haladnak a transzgénikus/génszerkesztős madárprojektek sokkal lassabban, hiszen minden manipulálni kívánt faj esetében meg kell oldanunk, hogy az ivari őssejteket fenntartsuk, azokat génszerkesszük, majd visszaültessük egy madárembrió fejlődő ivarszervébe, és majd csak ennek az állatnak az utódaiban fogunk esetleg látni valamit. A kazuár esetében még nem tudjuk, hogyan tudnánk fenntartani az ivari őssejteket, és figyelembe véve, hogy az állatnak öt évre van szüksége ahhoz, hogy ivarérett legyen, már önmagában annak az igazolása, hogy képesek vagyunk a kazuárgenomot szerkeszteni, 6-10 évbe telne, még ha most azonnal bele is csapnánk a dologba. Ha ezután egyszerre sikerülne is bevinni az összes korábban emlegetett módosítást, már akkor is a (túlzóan optimista) 11-15 évnél járnánk, de még mindig csak egy fogakkal és karmokkal rendelkező kazuárra lehetne büszke a bennünk lakó Dr. Wu.
Mert arról még egyelőre fogalmunk sincs, mi vezetett ahhoz, hogy a valamikori madárős farokcsigolyái összeforrtak egy pygostyle-nak nevezett csonttá. Bármennyit is tudunk a gerincesek farok fejlődéséről, még mindig nem tudunk eleget ahhoz, hogy egy madárembrióban ezt az evolúciós lépést visszafordítsuk. Az is árulkodó, hogy míg egy másik, a farkát nem olyan régen elvesztő fajban, az emberben időről időre előfordul egy-egy vesztigiális farok, csirkében ilyesmiről nem tudunk. Pedig lenne hol megjelenjen, hiszen az embernek köszönhetően mára a csirke lett a legnagyobb számban létező szárazföldi gerinces, és hogy egy ilyen milliárdos tömegben még senki nem szúrt ki egyetlen abnormálisan hosszú farokkal születő csirkét sem, az azt sugallja, hogy ez a folyamat nem fordítható vissza egykönnyen. (Hogy valami pozitívat is elmondhassunk, a közelmúlt egyik bizarr kísérlete, amelyben egy méretre szabott vécépumpára emlékeztető valamit tapasztottak kvázi farokként csirkékre, annyit legalább bebizonyított, hogy ha lenne farkuk, akkor a madarak inkább járnának úgy, ahogy azt a dinoszauruszokról sejtjük, vagyis itt pusztán a biomechanika diktálna egy viselkedésváltozást.)
És még ha a raptorfarok fogas kérdését meg is válaszolnánk, egy sokkal nagyobbal problémával találnánk szembe magunkat: bármennyire is dinoszauruszszerű lenne a génszerkesztett kazuárunk, „belül” továbbra is kazuár lenne. Úgy viselkedne és úgy táplálkozna, mint egy madár, vagyis magányos lenne és mindenevő, ami megint csak nem pont az, amit a Jurassic Park alapján várnánk tőle. A komplex viselkedés genetikája azonban olyan bonyolult kérdés, amit nemhogy 15, de még 25 év alatt sem fogunk megfejteni – arról nem is szólva, hogy a sok tízezernyi apró genetikai változás, amivel egy viselkedési program kialakulása járhat, azt jelentené, hogy ennyi helyen kellene nagyon pontosan szerkeszteni a genomot. Ez utóbbi önmagában is technológiailag megoldhatatlannak tűnik; ennél még az is valószínűbb, hogy 10-15 éves távlatban lehetségessé válik egy módosított kazuárgenomot valahogy egy csőben szintetikusan összeszerelni, ahogy az a GenomeProject-Write csapata ígéri, és aztán valahogy sikeresen bevinni egy madársejtbe, amiből ivari őssejtet hozunk létre.
Ezek együtt aztán eléggé egyértelműsítik, hogy 15 év múlva ugyanúgy 15 évnyire leszünk a Jurassic Park Max Hodak-féle „egzotikus új fajainak” víziójától, mint ahogyan folyamatosan 15-20 évre vagyunk az emberi Marsra szállástól is (hogy Elon Musk egy másik vesszőparipáját is elővegyük). Már ha nem érjük be egy megfelelően lenyírt tibeti masztiffal itt is. Ha fogadni kellene, személy szerint a Marsra szállást is sokkal közelebbinek tartom, mint hogy a filmbeli Isla Nubar víziója, akár kicsiben is megvalósuljon.
Max Hodak kijelentése így aztán vagy egyszerű PR-fogás – és mondjuk annak sikeres, hiszen mi is foglalkozunk vele –, vagy annak a legszebb példája, hogy milyen az, amikor valaki a Dunning–Kruger-görbe bal oldali csúcsán „hangosan gondolkodik”.
Az írás eredetileg a qubit.hu-n jelent meg.
Hány gén kell az élethez, vagy más szavakkal mi az a minimális genom, ami még lehetővé teszi, hogy egy sejt élni tudjon? Ez a viszonylag triviálisnak tűnő kérdés még mindig a legnehezebb kérdések egyike. Hiába szekvenáljuk és elemezzük most már ezrével a prokarióta élőlények genomjait, az utóbbi időben igazán nagy áttörést az elmúlt pár évben nem sikerült elérni. Ismerünk nagyon minimális genommal is fennmaradó parazita és szimbionta élőlényeket, de ezek gazdasejtjeiken kívül már nem életképesek, vagyis valamit elvesztettük abból a minimális génkészletből, ami az önálló élethez szükséges.
Az első emberi genom szekvenálásakor technológiai újításainak köszönhetően ismertté váló Craig Venter, pontosabban az általa alapított J. Craig Venter Institute (JCVI), most már több évtizede próbálja amolyan redukcionista eljárással meghatározni, hogy mi is lehet az a minimális genom, ami az élethez szükséges. Ez kb. azt jelenti, hogy fognak egy elég kis genomú baktériumot (esetükben a Mycobacterium mycoides-re esett a választás) és ebből próbálnak még kisebb genomú, de önállóan is életképes bakétriumot csinálni. Első próbálkozásuk inkább metodológiai érdekesség volt, ami azt bizonyította, hogy egy (ismert szekvenciájú) teljes genomot is meg lehet szintetizálni és aztán csak abból kiindulva is egy teljes értékű sejt jöhet létre.
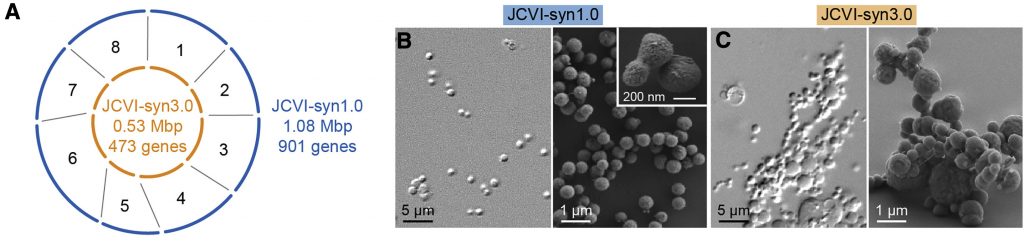
Fél évtizeddel később aztán bejelentették, hogy elkészült a JCVI-Syn3.0, ami már valóban fontos lépés volt a genom-minimalizálás felé, hiszen az M. mycoides genom eredeti 901 génjéből több százat kiszórtak és végül 473 maradt. A Sny3.0 kétségtelenül élt, de ahogy akkor is tudni lehetett, azért egy picit “magyar narancs” jellegű volt, osztódási nem mindig voltak szimmetrikusak, gyakran nagy vakuólák, máskor filamentózus szerkezetek jelentek meg a tenyészetekben.
Most ennek a furcsaságnak mentek utána a JCVI és az amerikai Nemzeti Standardok és Technológia Intézet (National Institute of Standards and Technology – NIST) kutatói. A munkában modern mikrofluidikai berendezéseket használtak a fura sejtmorfológiák pontos jellemzésére és a kísérlet alapját az képezte, hogy visszamentek megvizsgálni azokat a köztes állapotokat, amelyek a Sny3.0 létrehozásakor találtak – ti. akkor a Syn1.0 genomot nyolc részre osztották és az egyes részekből párhuzamosan vágták ki a nem esszenciális géneket, majd a nyolc “minimál” genomdarabot egyesítették a Syn3.0 genomjába.
Most a kutatók először arra figyeltek fel, hogy a furcsán viselkedő fenotípus már akkor megjelenik, ha Syn1.0 genomban a 6. szegmenst helyettesítjük a minimál-szegmenssel (RGD6), illetve fordítva, ha a Syn3.0-ban a hatodik szegmenst egy nagyobbra cseréljük vissza, akkor megint normálisan viselkedő sejteket kapunk (ez lett a JCVI-Syn3A). (A Syn1.0 és Syn3.0 genomok közt a hatodik szegmensben 76 génnyi különbség van, de itt elég volt egy fragmenst visszapótolni, amiben 19 plussz gén van.)
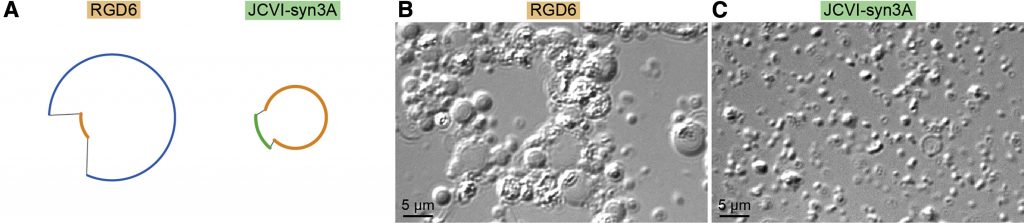
Vagyis adta magát, hogy a szóban forgó hatodik szegmenst, pontosabban az abból kitörölt géneket kell még részletesebben megnézni, hogy megérthessük, miért nem osztódik normálisan egy JCVI-Syn3.0 sejt.
Ahogy az alábbi táblázat is mutatja, összesen 19 gén különbözik a Syn3.0 és Syn3A genomok között, amelyeket nyolc további alszegmensbe (klaszterbe) lehetett osztani. Ezek közt voltak olyanok (pl. riboszomális RNS-eket kódoló gének), amelyek eredetileg is azért töröltek, mert redundánsak, vagyis több kópiában is jelen vannak a genomban, így nem volt meglepő, hogy ezek visszapótlása a Syn3.0 genomba nem okozott változást, a sejtosztódások továbbra is furák maradtak.
De volt pár másik, mint pl. az ftsZ, amelynek a fehérjeterméke (egy tubulin jellegű fehérje) korábban is ismerten fontos szerepet játszik a sejtosztódásban. Nem túl nagy meglepetésre, az ftsZ fontosnak bizonyult a normális morfológiához. Végül összesen 7 olyan gént azonosítottak, amelyek így vagy úgy, de együtt bepótolva a Syn3.0 genomba biztosították a normális osztódást.
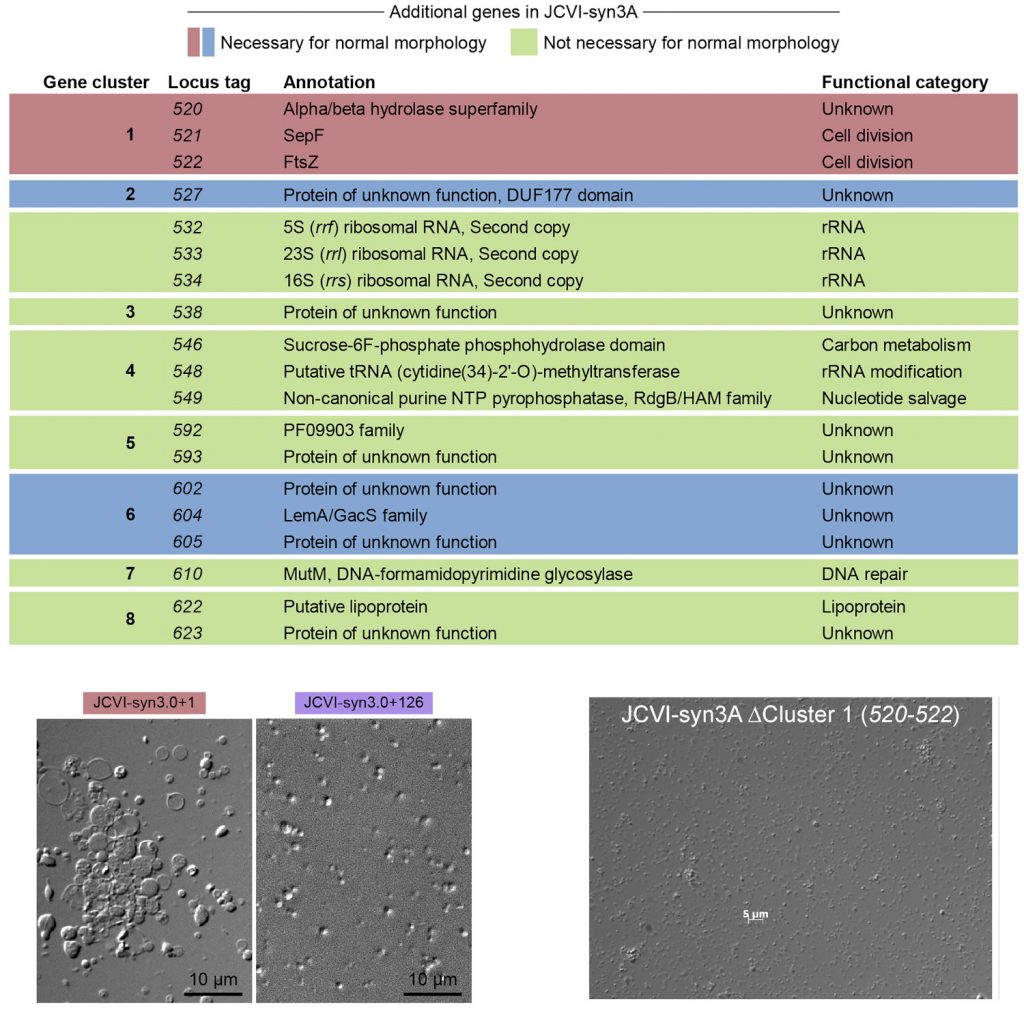
A történet itt véget is érne, de azért még van két érdekesség, amit mindenképpen megemlítenék: egyrészt, hogy ebből a mindössze 7 db. génből is öt olyan, aminek nem ismerjük az igazi funkcióját. És amikor egy tényleg alig pár száz génből álló genom esetében is egy ilyenbe belefutunk, akkor az mindig kellő perspektívába teszi, hogy a saját, sokkal komplexebb és közel húszezer fehérje-kódoló gént tartalmazó genomunkat mennyire érthetjük per pillanat.
A másik fontos dolog, hogy néha az egyszerű dolgok sem egyszerűek. Például bármennyire is fontosnak tűnik, de nem elegendő, ha csak az ftsZ-t tartalmazó klasztert visszük vissza a Syn3.0 genomjába, hanem a hét említett génre együtt van szükségünk a normális fenotípushoz. Ugyanakkor, ha a Syn3A genomból indulunk ki és abból töröljük ki az ftsZ-t és két további esszenciális(nak tűnő) gént tartalmazó klasztert, akkor a morfológia továbbra is normális marad. Vagyis a Syn3.0 genomon végzett “visszapótlási kísérletben” nem esszenciálisnak bizonyuló tizenkét génnek (köztük szintén van három ismeretlen funkcióval) valamiképpen kompenzálnia kell tudnia ennek a három génnek a hiányát. Hogy hogyan valósul meg ez a redundancia, azt még ötlet szintjén sem tudjuk.
És ez az, ahol a technológia tour de force, amire a JCVI kutatói mindig is hajlamosak, önmagában nem tud segíteni. Mert itt van ugyan egy minimális genom, de még mindig olyan alapvető kérdésekre is keressük a választ, hogy egyes esszenciális gének miért is annyira fontosak.
(A borítókép a J. Craig Venter Institute oldaláról származik.)
Pelletier JF, Sun L, Wise KS, Assad-Garcia N, Karas BJ, et al. (2021) Genetic requirements for cell division in a genomically minimal cell. Cell doi: 10.1016/j.cell.2021.03.008.
A Budapest Science Meetup égisze alatt kisebb-nagyobb rendszerességgel rendelkező Karanténnaplókban egyébként is igyekszünk a lehető legnaprakészebb információkat összeszedni, de a friss Karanténnaplónk vendége, Pardi Norbert maga is részt vett Karikó Katalin oldalán az mRNS vakcinák kifejlesztésében, így talán a CriticalBiomass olvasóinak is érdekesebb lehet a beszélgetés (a beágyazott videó a teljes Karanténnapló kb. közepén indul, az interjú elején).
Tegyük fel a szándékosan provokatív kérdést, hogyan lehetne megduplázni az ország bruttó nemzeti össztermékét (GDP)? Ez jelenleg 163,5 milliárd USD, ha úgy tetszik az egy főre jutó GDP 16470 USD, ezzel a világon az ötvenegyedikek vagyunk. Ha megkétszereznénk a bruttó nemzeti összterméket, akkor körülbelül Olaszország szintjére jutnánk. De hogyan lehetne ezt megtenni? Nyilván ha olajat, uránt, lítiumot vagy aranyat találnának nagy mennyiségben mondjuk az Alföldön, az segítene, de erre nem sok esélyt látok. Így mindenképpen valamilyen ipari teljesítménnyel kellene ezt megtenni. Erre tennék egy meglepő javaslatot: Gyárthatnánk fehérjéket.
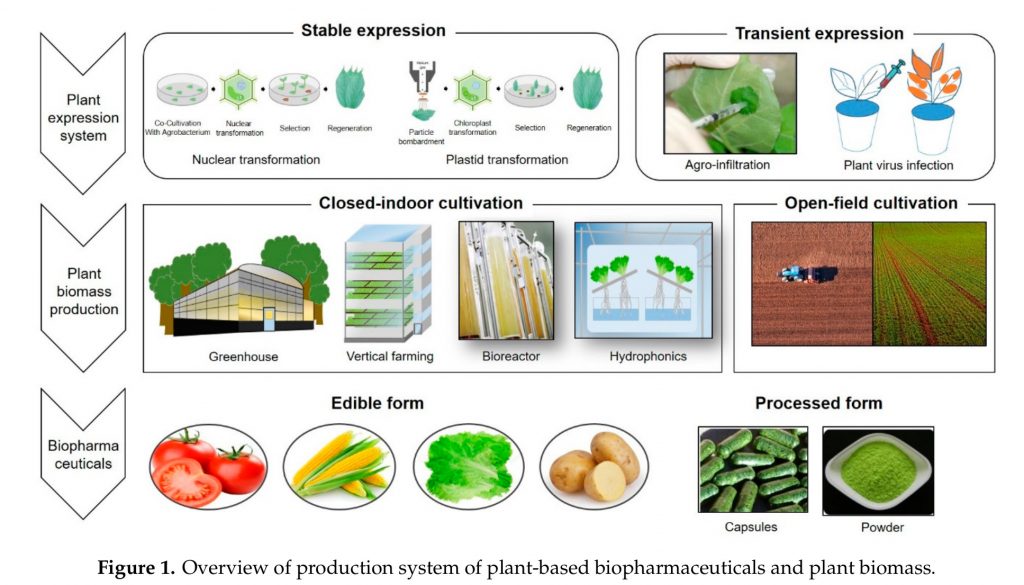

Kínában a génmódosított növények helyzete sokáig kifejezetten mostohának számított: Bár több, mint hatvan génmódosított növény behozatalát és fogyasztását engedélyezték, termesztési engedélyt csak nagyon kevés fajta kapott. Azonban úgy tűnik, ez hamarosan megváltozik.
Egy kattintás ide a folytatáshoz….Az USA elnökválasztásában oroszlánrészt játszott a Regeneron nevű cég gyógyszere. Ugyanis Donald Trump elnök néhány héttel a választások előtt elkapta a Sars-CoV-2 vírust, ám annak ellenére, hogy már hetven éves is elmúlt, napok alatt kigyógyult belőle, különösebb tünetek nélkül. Gyors fölépülésében valószínűleg nagyban segített a kezelés. De adódik a kérdés, hogy ha létezik ilyen hatékony gyógyszer a COVID19 -re, akkor miért nem kaphat mindenki a szerből, amiből az elnök?
Egy kattintás ide a folytatáshoz….Az antibiotikumoknak ellenálló baktériumok az egészségügy egyik komoly kihívása, nem véletlenül próbálkoznak jó páran új elven működő baktériumölő szerek készítésével. Egy friss cikk viszont igazi különlegesség: az első és utolsó szerzői a Szegedi Biológiai Kutatóközpontban és a Ljubljanai Egyetemen dolgoznak, igazi európai fejlesztésről beszélhetünk hát.