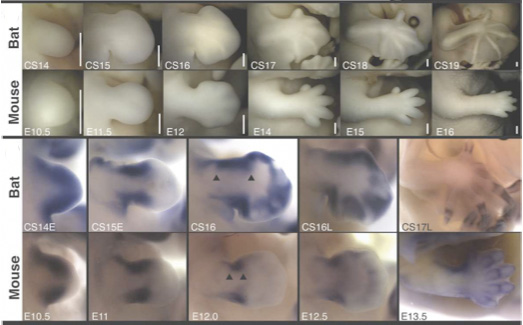
 Laikusok számára talán meglepő módon, az Onthophagus genusba tartozó trágyabogarak azon fajok közé tartoznak, amelyeken a legjobban lehet az evolúció menetét tanulmányozni. S ezt nemcsak a különböző fajok hímjeinek fején díszelgő szarvak sokfélesége teszi lehetővé, hanem az is, hogy egy-egy fajon belül a különböző hímek eltérő stratégiákat alkalmaznak génjeik továbbörökítése végett.
Laikusok számára talán meglepő módon, az Onthophagus genusba tartozó trágyabogarak azon fajok közé tartoznak, amelyeken a legjobban lehet az evolúció menetét tanulmányozni. S ezt nemcsak a különböző fajok hímjeinek fején díszelgő szarvak sokfélesége teszi lehetővé, hanem az is, hogy egy-egy fajon belül a különböző hímek eltérő stratégiákat alkalmaznak génjeik továbbörökítése végett.
A szarv nemcsak dísz, de fegyver is: a nőstényekért vívott ádáz csata eszköze. S mivel mérete általában igen tiszteletreméltó (az állat testéhez képest mindenképpen), értelemszerűen sok energiát igényel létrehozása. Éppen ezért, egy olyan közösségben, ahol nagy a „népsűrűség”, s így a hímeknek különösen ádáz csatákban kell a rátermettségüket bizonyítani, hiábavaló olyan szarvakat létrehozni, amelyek szub-optimális méretűek. Viselőjük a csatákban nem nyerhetne, viszont ugyanazt az energiamennyiséget, más értelmesebb célokra is fordíthatná.
Például nagyobb szemek és/vagy herék kialakítására, amelyek nem lennének teljesen hiábavalók, hiszen a nőstények elnyerésének és így az utódok biztosításának „lovagias” módja mellett, van egy „sunyi”, lopakodó verziója is, ahol a hímek meghátrálnak a nyílt harc elől, viszont a járatok mélyében, ha esélyük nyílik rá gyorsan mégis párosodnak a nőstényekkel.
Vagyis, elméletileg, megéri némi extra energiát a párzó szervre (ami ez esetben aedeagus néven fut) pazarolni, hiszen egy nagyobb méretű aedegus mélyebbre tudja juttatni a hím ivarsejtjeit, így még ha a nőstény később párosodik is egy nagy szarvú „alfa hímmel”, jó eséllyel a szarvatlan hím lesz a következő nemzedék atyja. (A szarv és a párzószerv egyaránt az embrionális fejlődés egy olyan szakaszában jön létre, amikor a bogár nem táplálkozik, így csak véges mennyiségű energiaforrás áll a rendelkezésére.)
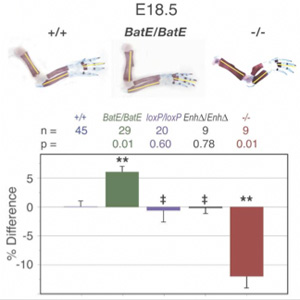
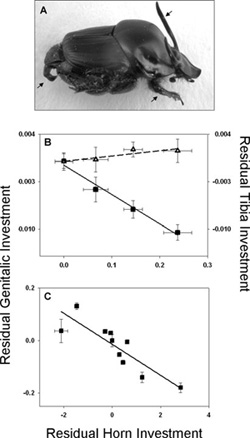
S hogy ez mennyire így működik a valóságban arra jó példa a Dél-Európában őshonos Onthophagus taurus, amelyet olyan 50 évvel ezelőtt telepítettek be az Egyesült Államok keleti partvidékére, illetve Ny-Ausztráliába. A különböző területeken a bogár különböző sűrűségeket ért el: Amerikában elég szellősen éldegélnek az egyedei, míg Ausztráliában sűrűn fordulnak elő. Az eltérő egyedszám öt évtized alatt jól látható eltéréseket hozott létre a különböző populációkban: előbbi helyen közel minden hím szarvat visel, míg utóbbi helyen csak a legnagyobbak. Az aedeagus mérete viszont az amerikai populációk esetében lényegesen kisebbnek bizonyult, mint az ausztrálok esetében, vagyis a hímek egyszerűen más stratégia szerint élnek a világ két sarkán (lásd még B ábra, fekete négyzetek): egyik helyen a párzó szervbe fektetik az energiát, a másik helyen viszont a nőstények elnyerésére szolgáló szarvakba. (Fontos, hangsúlyozni, hogy a szarvak csökkenése nem az állat általános növekedését okozza, mert például a lábízületük – ezt jelölik a B ábra háromszögei – relatív mérete nem mutat az aedeagushoz hasonló változást.)
Slusszpoén, hogy ez az összefüggés nemcsak az O. taurus populációi esetében figyelhető meg, de különböző Onthophagus fajok vonzatában is (C ábra): a szarv és az aedeagus mérete fordítottan arányos. Evolúciós léptékkel csak az számít, hogy kinek mennyi utódja lesz. Hogy ki miként éri el a célját, már részletkérdés.
Parzer HF, Moczek, AP (2008) Rapid antagonistic coevolution between primary and secondary sexual characters in horned beetles. Evolution doi: 10.1111/j.1558-5646.2008.00448.x

 A görög mitológia
A görög mitológia  Az állatvilágban közel sem szokatlan, ha egy-egy faj egyedei már embrionális fejlődésük után, de még felnőtté válásuk előtt nagyarányú változáson esnek át (gondoljunk csak a lábat növesztő ebihalakra), a
Az állatvilágban közel sem szokatlan, ha egy-egy faj egyedei már embrionális fejlődésük után, de még felnőtté válásuk előtt nagyarányú változáson esnek át (gondoljunk csak a lábat növesztő ebihalakra), a 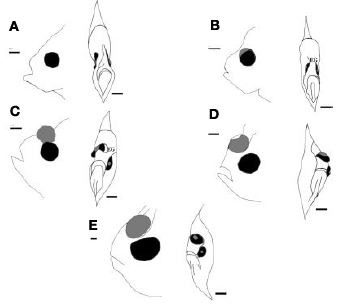 A vándorlás kapcsán azért indokolt a jelenidő, mert ezt a folyamatot minden egyes halnak le kell „játszania” élete során – ugyanis a lepényhalak életük kezdetén még igencsak „normálisak”, s szemük a test két oldalán helyezkedik el (jobb oldali ábra, A). Igaz, ezek a fiatal halak még függőleges testhelyzetben úszkálnak, s ezen viselkedésük is csak a fizikai átalakulásuk, ún. metamorfózisuk (B-E) végére változik meg.
A vándorlás kapcsán azért indokolt a jelenidő, mert ezt a folyamatot minden egyes halnak le kell „játszania” élete során – ugyanis a lepényhalak életük kezdetén még igencsak „normálisak”, s szemük a test két oldalán helyezkedik el (jobb oldali ábra, A). Igaz, ezek a fiatal halak még függőleges testhelyzetben úszkálnak, s ezen viselkedésük is csak a fizikai átalakulásuk, ún. metamorfózisuk (B-E) végére változik meg.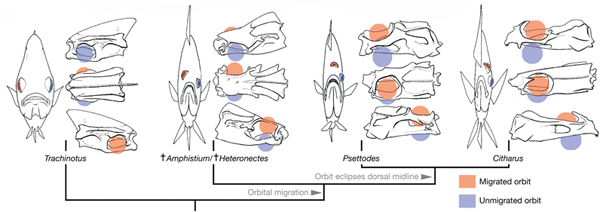
 Ha egyszer majd valaki veszi a fáradtságot, hogy összeállítsa, a legfélrevezetőbb magyar állatnevek listáját, a lándzsahal mindenképpen előkellő helyre fog befutni. Ugyanis ez a kis állat nem hal, de mégcsak nem is gerinces. Ettől persze a hasonlóság még valós, de közel sem annyira szoros rokonságot takar (mint látni fogjuk, sőt), mint azt a nevezéktan sugallja.
Ha egyszer majd valaki veszi a fáradtságot, hogy összeállítsa, a legfélrevezetőbb magyar állatnevek listáját, a lándzsahal mindenképpen előkellő helyre fog befutni. Ugyanis ez a kis állat nem hal, de mégcsak nem is gerinces. Ettől persze a hasonlóság még valós, de közel sem annyira szoros rokonságot takar (mint látni fogjuk, sőt), mint azt a nevezéktan sugallja. A kreacionisták egy szűnni nem akaró tévedése/csúsztatása az evolúcióval kapcsolatban, hogy a folyamatnak teljesen véletlenszerű a kimenetele. Ez persze ebben a formában merőben hamis, hiszen maga a természetes szelekció egy nagyon is rigorózus válogatás során „dönti el”, hogy adott faj mely egyedei talpraesettebbek adott körülmények között, ugyanakkor annyi igazságmag azonban van benne, hogy magának az evolúciós mechanizmusnak létezik egy véletlen komponense is. Ez pedig nem más, mint azoknak a változatoknak a létrejötte, amelyekből a szelekció később „válogat”.
A kreacionisták egy szűnni nem akaró tévedése/csúsztatása az evolúcióval kapcsolatban, hogy a folyamatnak teljesen véletlenszerű a kimenetele. Ez persze ebben a formában merőben hamis, hiszen maga a természetes szelekció egy nagyon is rigorózus válogatás során „dönti el”, hogy adott faj mely egyedei talpraesettebbek adott körülmények között, ugyanakkor annyi igazságmag azonban van benne, hogy magának az evolúciós mechanizmusnak létezik egy véletlen komponense is. Ez pedig nem más, mint azoknak a változatoknak a létrejötte, amelyekből a szelekció később „válogat”.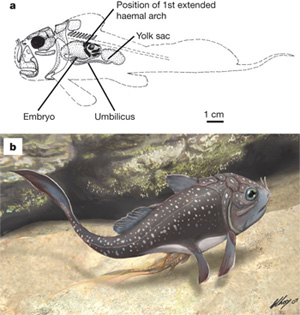 Ha a halak szaporodásáról beszélünk, az értő akvaristáktól eltekintve, a legtöbb ember szemei előtt az aljzaton hagyott ikrák és tovaúszó anyák jelennek meg. Tegyük hozzá, természetesen nem alaptalanul, hiszen a szaporodás ezen, a mi szemszögünkből nézve kicsit mostoha módja a leggyakoribb a halak körében. Sikeréhez persze elengedhetetlen az embrióhoz „útravalóul” csomagolt nagy mennyiségű szikanyag, hogy szegény utód mégse éhezzen, amíg képessé nem válik a saját táplálékszerzésre.
Ha a halak szaporodásáról beszélünk, az értő akvaristáktól eltekintve, a legtöbb ember szemei előtt az aljzaton hagyott ikrák és tovaúszó anyák jelennek meg. Tegyük hozzá, természetesen nem alaptalanul, hiszen a szaporodás ezen, a mi szemszögünkből nézve kicsit mostoha módja a leggyakoribb a halak körében. Sikeréhez persze elengedhetetlen az embrióhoz „útravalóul” csomagolt nagy mennyiségű szikanyag, hogy szegény utód mégse éhezzen, amíg képessé nem válik a saját táplálékszerzésre.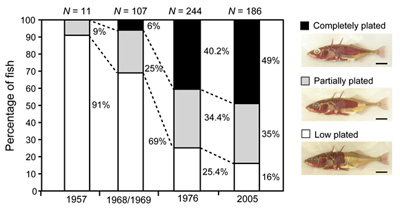 Az élőlények környezetének változásaira a természetes szelekció olyan génvariánsok (allélok) elterjesztésével reagál, amelyek az új körülmények között a legtöbbet nyújthatják hordozójuknak. És mivel a környezet folyamatosan változik, elvétve még az is előfordulhat, hogy hirtelen egy új és frissen elterjedt allél már nem előnyösebb, mint a gén régebbi verziója, sőt, s ilyenkor tanúi lehetünk egyfajta természetes „vissza az egész” procedúrának. Ezt a szaknyelv „reverz evolúciónak” nevezi és a közelmúltban a tüskés pikók egy populációjának esetében figyelték meg.
Az élőlények környezetének változásaira a természetes szelekció olyan génvariánsok (allélok) elterjesztésével reagál, amelyek az új körülmények között a legtöbbet nyújthatják hordozójuknak. És mivel a környezet folyamatosan változik, elvétve még az is előfordulhat, hogy hirtelen egy új és frissen elterjedt allél már nem előnyösebb, mint a gén régebbi verziója, sőt, s ilyenkor tanúi lehetünk egyfajta természetes „vissza az egész” procedúrának. Ezt a szaknyelv „reverz evolúciónak” nevezi és a közelmúltban a tüskés pikók egy populációjának esetében figyelték meg. A bordás- (vagy fésűs) medúzákat, vagyis a
A bordás- (vagy fésűs) medúzákat, vagyis a 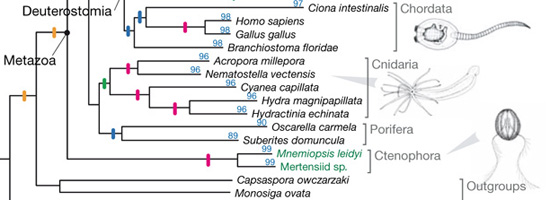
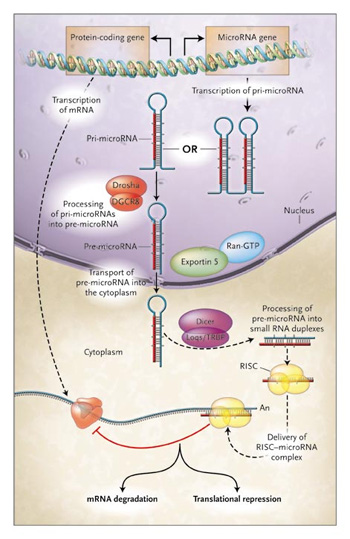 Bő tíz éve szinte véletlen megfigyelésekből indult a dolog és mára a biológia egyik legizgalmasabb területévé vált az RNS-függő génexpresszió-szabályozás tanulmányozása. Felfedezőinek máris
Bő tíz éve szinte véletlen megfigyelésekből indult a dolog és mára a biológia egyik legizgalmasabb területévé vált az RNS-függő génexpresszió-szabályozás tanulmányozása. Felfedezőinek máris