Ha szelvényes állatok kerülnek szóba, akkor elsőre legtöbben jó eséllyel az ízeltlábúakra gondolnak majd. Nem véletlenül persze, hiszen egy százlábún, vagy egy folyami rákon nem lehet nem észrevenni a jól kifejlett, kvázi ismétlődő egységetket, szaknevükön szegmenseket. Pedig, az az igazság, hogy saját közelebbi rokonságunk is szelvényezett, s ha ezt nehéz lenne elképzelni, gondoljunk csak a “gerincesek” névadó szervére. Egy emberi gerincoszlop számos (egész pontosan 24), hasonló felépítésű egységből épül fel: 7 nyaki, 12 háti és 5 ágyéki csigolyából (meg persze még van az 5, ill. 4-6 csigolya összeforrásából létrejövő keresztcsont és farokcsont, de ezek épp keletkezésük miatt – emberben – álcsigolyának számítanak). A háti csigolyák esetében, a hozzájuk kapcsolódó bordák révén a “szelvényesség” talán még evidensebb, de valószínűleg azért senkit nem kell külön meggyőzni, hogy egy nyaki- és ágyéki csigolya valójában “variáció egy témára”.
A gerinces szelvényesség abszolút bajnokai értelemszerűen a kígyók, akik a maguk 300+ csigolyájával egész nagyságrendet vernek az emlősökre, halakra és madarakra, és még a kétéltűek és más üllők között is alig lelünk valakit, aki egyáltalán a közelükbe érhetne. A kígyók testalkata alapján a naiv szemlélő azt is hihetné, hogy ez az extrém csigolyaszám a farok megnyúlásának köszönhető, de a “józan paraszti ész” ezúttal tévútra vinne. Ugyan a siklók és társaik szépszámú (kb. 70) farokcsigolyával büszkélkedhetnek, a csigolyák elsöprő többsége a háthoz tartozik. Ennek megfelelően mindegyiken egy-egy pár borda díszeleg, s csak azok után lelhetjük fel a hátsó végag csökevényeit, már ahol még ezek kivehetőek – lásd boák (de pl. fosszilis kígyókban azért elég egyértelműek). Elsőre talán egy kicsit paradox módon, nyakcsigolyából mindössze három van, de ennek az oka pont abban keresendő, hogy bizonyos korai fejlődési mintázatok úgy változtak meg, hogy a kígyók mellső végtagjai nem is kezdenek kialakulni.
Ha a csigolya-, pontosabban szegmens szám növekedés nyomába akarunk eredni, akkor a kígyók egyedfejlődésének egész korai stádiumához kell visszamennünk, pontosan addig, amíg ezek a szegmensek el nem kezdenek kialakulni. A csigolyák és a hozzájuk tapadó izmok szomitának nevezett mezodermális eredetű szövetblokkokból jönnek létre, és a szelvényességük későbbi titka abban keresendő, hogy már maguk a szomiták is szegmentáltak. A szomiták kialakulásának (vagyis a szomatogenezisnek) kezdetén egy kígyó embrió nem nagyon különbözik a többi gerincestől. Csak ezután válik fokozatosan evidenssé a különbség, ui. míg a legtöbb gerincesnél néhány tucat tucat szomita kialakulása után a folyamat leáll, a kígyók szelvényei csak egyre keletkeznek. Hogy megértsük, ennek mi is az oka, ahhoz először tisztázni kell, hogy pontosan mi is zajlik egy gerincesben a szomatogenezis során.
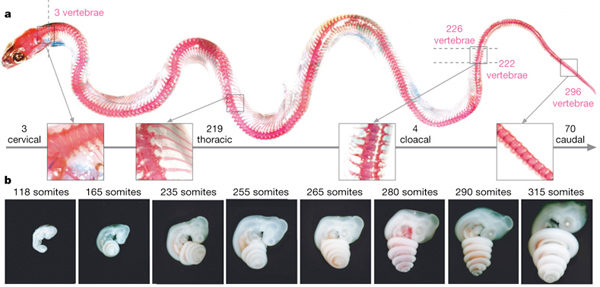
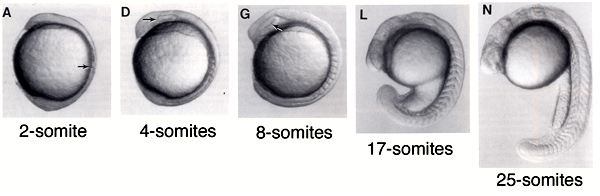
Ehhez pedig a zebrahalakat fogjuk használni, részint mert így rámnyomható a szakmai sovinizmus bélyege, részint pedig azért, mert ez a szomatogenezis szempontjából az egyik legjobban jellemzett modelállat. A halak szomitái a fejlődés 11. órájának környékén kezdenek kialakulni és ezután tempósan, jól megjósolható félórás iődközönként keletkezik egy-egy újabb szegmens, míg ki nem alakul mind a 31. A szomiták száma annyira jellemző az embriogenezis ezen szakaszában a halak fejlődésére, hogy az egyes fejlődési stádiumokat a számuk alapján nevezték el (lásd alábbi ábra).
A szomitogenezis mindig az elülső (fejhez legközelebbi) szegmens kialakulásával indul, a többi pedig fokozatosan adódik hozzá. Mindeközben a szomiták, ill. az embrió farki vége között egy differenciálatlan, és méretében egyre csökkenő szövetdarabot figyelhetünk meg. Ez szaknyelven a poszt-szomitikus mesoderma (post somitic mesoderm – PSM) és az itt lelhető sejtekben játszódnak le mindazok a folyamatok, amelyek nélkül nem jöhetnek létre a szomiták.
Mielőtt azonban beleásnánk magunkat a PSM molekuláris rejtelmeibe, egy kis kitérőt teszek, hogy nagyvonalakban felvázoljam, miként tanulmányoznak a biológusok egy olyan komplex folyamatot mint a szomatogenezis.
A legelső gond gyakran az, hogy nem is igen tudjuk, hogyan kezdjünk a jelenség leírásához: nem ismert semmi a folyamatról, fogalmunk sincs, milyen gének szerepelnek benne. A problémát kiküszöbölendő, olyan mutánsokat kezdünk keresni, amelyekben a vizsgált folyamat hibásan zajlik le. Szerencsére (ebből a szempontból…) ma már nagyszámú kémiai mutagén ismert, s így nem kell csak a természetre hagyatkozzunk (mivel nagyon sok mutáció eleve lehetetlenné teszi, hogy hordozója elérje az ivarérett kort, ez kifejezetten szerencse is). A folyamat viszonylag egyszerű: egy halat pár napig mutagén fürdőben tartunk, így az ez idő alatt kialakuló ivarsejtjei közt számos olyan lesz, amely mutációt hordoz. A következő lépésben aztán a hal utódjai közül kiszűrjük azokat, amelyekben az általunk vizsgált folyamat gallyra ment és egy kis vidám genetikai térképezés után, máris “kezünkben lesz” a jelenségben ludas gén.
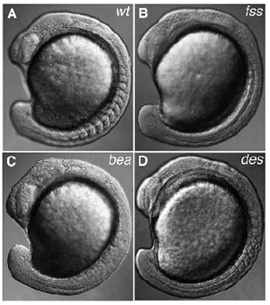
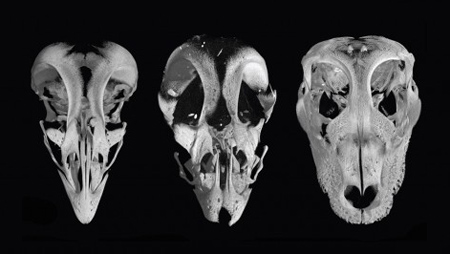
Zebrahalakban az első nagy mutagenezis screeneket (mert ez a fent körülírt tevékenység hivatalos neve) még a kilencvenes évek közepén ejtették meg és már ekkor számos olyan mutánst leltek, ahol a szomatogenezissel kisebb-nagyobb gondok adódtak. A mellékelt ábrán lehet néhány ilyent látni (wt = normális, “vad” típus; fss = fused somites; bea = beamter; des = deadly seven), s ezek közül sokról (pl. bea és des) kiderült, hogy ugyanannak a jelátviteli útvonalnak, a Notch-Delta szignáltranszdukciós folyamatnak a résztvevői.
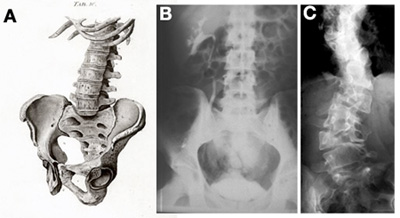 Ez az útvonal egyébként a gerincesekben univerzálisan fontos szereppel bír a szegmentáció kialakulásában (a mikéntről lásd egy picit alább). Mi sem mutatja ezt talán jobban, mint hogy számos olyan emberi betegség esetében, ahol az egyik tünet a gerincoszlop abnormális alakjában nyilvánul meg, a hibás génről kiderült, hogy valamit a Notch útvonallal kavar.
Ez az útvonal egyébként a gerincesekben univerzálisan fontos szereppel bír a szegmentáció kialakulásában (a mikéntről lásd egy picit alább). Mi sem mutatja ezt talán jobban, mint hogy számos olyan emberi betegség esetében, ahol az egyik tünet a gerincoszlop abnormális alakjában nyilvánul meg, a hibás génről kiderült, hogy valamit a Notch útvonallal kavar.
A jobboldali ábra C paneljén látható beteg esetében (A-n a gerincoszlop ágyékövi részének vázlata látszik egészséges emberben, B-n ugyanez egy röntgenfelvételen) a delta-like 3 gén mutációja okozta az elváltozást.
Mindezen kis kitérő után akkor végre lássuk, hogy mi is folyik a PSM “boszorkánykonyhájában”. Még a molekuláris fejlődésbiológia ’80-as években kezdődő forradalmi változásai előtt számos elmélet született,
megmagyarázandó, mi is zajlik szomitogenezis közben. Az igazsághoz legközelebb Jonathan Cooke és Christopher Zeeman jutottak, akik egy 1976-os cikkükben vázolták fel az “óra és hullámfront” (“clock-and-wavefront”) modellt (hogy ez pontosan mi is, az remélhetőleg kiderül a következő bekezdésekből). A modell valós életben való relevanciájának bizonyításában elévülhetetlen érdemeket szerzett, a poszt apropójaként szolgáló kígyós cikket is jegyző, Olivier Pourquié.
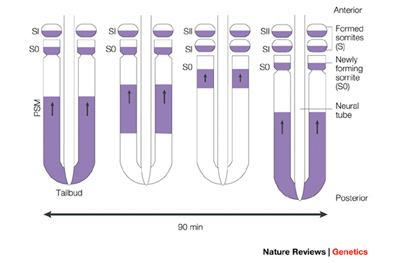
Pourquié és kutatócsoportja számos olyan gént izolált, amelyek igen dinamikus fejeződnek ki a PSM-ben. Egy szomita-képződési ciklus alatt (ami, mint írtam zebrahalakban kb. félóra, de más fajokban lehet egy-, vagy másfél óra is, attól függően milyen a szóbanforgó élőlény átlagos növekedési sebessége) ezek a gének előbb a PSM leghátsó, farok körüli részén expresszálódnak, majd fokozatosan egyre előrébb levő sejtekben – miközben a hátsó sejtekben megszűnik a gén kifejeződése -, mígnem a már kialakult szomiták alatti sejtekben elhal a “hullám”. A ciklus ezután újra indul, ám ezen utóbbi sejtek már nem vesznek részt benne, mert belőlük lesz az új “legutolsó” szomitapár.
A folyamat értelmezéséhez fontos kiemelni, hogy itt nem sejtek vándorolnak, hanem csak egy gén kifejeződése fut végig egy sejthalmazon. Ha lebontjuk a jelenséget az egyes sejtek szintjére, akkor már nem egy “hullámmal” állunk szemben: arról van szó, hogy egy-egy sejt bizonyos periodicitással elkezdi kifejezni a szóbanforgó géneket, majd kikapcsolja azokat. Hogy a rendszer flottul működjön (és a szövet szintjén a “hullámot” produkálja), ahhoz két dolog elengedhetetlen: legyen a sejteknek valami belső órája, egy ún. oszcillátora, ami ezt a periodicitást képes produkálni, illetve a szomszédos sejtek valamiképpen kommunikálni tudják egymással, hogy a ciklus melyik szakaszában vannak – hiszen ha minden sejt a maga feje után pörög, akkor abból előbb-utóbb káosz lesz és nem egy szabályos hullámfront.
A molekuláris óra mibenléte még nem teljesen tisztázott, de a legtöbben arra teszik a pénzüket, hogy egy egyszerű negatív-feedback ciklusról van szó: az óra gén-ről (amit csak a példa kedvéért hívunk így, mert nem tudjuk pontosan mi ez) átíródik a megfelelő RNS, majd erről elkészül az ÓRA fehérje, ami kikapcsolja saját génjének működését. Így azonban persze nem keletkezik több ÓRA fehérje, a sejt természetes belső mechanizusai pedig adott időn belül elbontják a már meglevő ÓRA fehérjéket (ezt nevezzük fehérje turnover-nek), így előbb utóbb a gén felszabadul a gátlás alól. És kezdődik minden elölről. Ha a fehérje átíródás és lebomlás megfelelő ütemben zajlik, már meg is van a kívánt periodicitás. (Az ínyencek kedvéért: az óra gén szerepre leggyakrabban a hes1 és hes7 géneket jelölik.)
A sejtek összehangolásáról már többet tudunk – itt kerül a képbe a korábban emlegetett Notch -Delta jelátvitel. Szomszédos sejtek ezen útvonal segítségével hangolják össze egymás belső ciklusát, így persze érthetővé válik, hogy mi is okozta a mutánsok fura kinézetét: fejlődésük során az egységesítés hiányában a belső ciklusok lassan elállítódtak, a hullámfront egyre szabálytalanabbá vált, a kialakuló szomiták meg egyre kuszábbakká.
A PSM sejtjeinek belső órája mindaddig ketyeg, amíg a már kialakult szomiták nagyon közel nem kerülnek az embrió hátsó részéhez (ahonnan a hullám indul). Ekkor, feltehetőleg az “érett” szomitákból kibocsájtott retinolsav (retinoic acid – RA) ellensúlyozza a PSM sejtjeinek korábbi állapotát biztosító FGF- és Wnt jelátviteli rendszerek aktivitását, és a belső oszcillátorok kikapcsolnak.
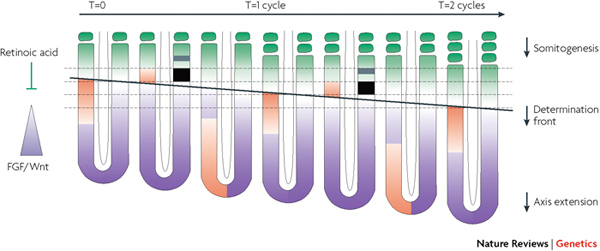
Na, akkor mindezeket tisztázva már csak tényleg arra kellene válaszolni, hogy mi is történik a kígyókban. A rendszer logikájából látható, hogy alapvetően két út kínálkozik a szomiták számának megnövelésére: vagy a PSM méretét növeljük meg (pl. több sejtosztódással), hogy több szomitára elegendő sejt legyen benne, vagy pedig az órát turbózzuk fel, hogy gyorsabban “ketyegjen”.
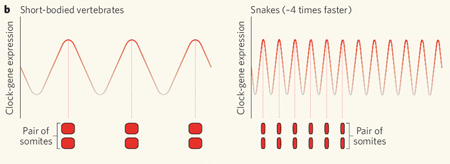 A kígyók a két megoldás ötvözetét használják, bár a hangsúly az nagyon is az utóbbin van. A csirkék 16 és az egerek 13 db. sejtosztódásával szemben a kígyó PSM 21 sejtosztódáson megy keresztül. Szignifikáns különbség, de koránt sem akkora, hogy a nagyságrendnyi különbségért felelős lehessen. Sokkal inkább alkalmas erre a négyszer gyorsabban ketyegő sejtóra. Ez természetesen négyszer gyorsabb hullámokat idéz elő, amelyek így, egységnyi fejlődési idő alatt (vagyis más szervek fejlődéséhez viszonyítva), négyszer annyi szomitát hoznak létre, mint a rövid testű gerincesek, pl. zebrahalak – bár így a szomiták mérete lesz kezdetben kicsi.
A kígyók a két megoldás ötvözetét használják, bár a hangsúly az nagyon is az utóbbin van. A csirkék 16 és az egerek 13 db. sejtosztódásával szemben a kígyó PSM 21 sejtosztódáson megy keresztül. Szignifikáns különbség, de koránt sem akkora, hogy a nagyságrendnyi különbségért felelős lehessen. Sokkal inkább alkalmas erre a négyszer gyorsabban ketyegő sejtóra. Ez természetesen négyszer gyorsabb hullámokat idéz elő, amelyek így, egységnyi fejlődési idő alatt (vagyis más szervek fejlődéséhez viszonyítva), négyszer annyi szomitát hoznak létre, mint a rövid testű gerincesek, pl. zebrahalak – bár így a szomiták mérete lesz kezdetben kicsi.
Hogy mindennek mi a közvetlen genetikai oka, azt még nem tudjuk. Ugyanakkor érdekes látni, hogy a végtegfejlődés modulja mellett, a kígyók esetében az evolúció egy másik fejlődési modullal is vidáman (és eredményesen) “kísérletezgetett”.
Gomez C, Ozbudak EM, Wunderlich J, Baumann D, Lewis J, Pourquié O (2008) Control of segment number in vertebrate embryos. Nature 454: 335-339.
Vonk FJ, Richardson MK (2008) Developmental biology: Serpent clocks tick faster. Nature 454: 282-283.
Dequéant ML, Pourquié O (2008) Segmental patterning of the vertebrate embryonic axis. Nat Rev Genet 9(5): 370-382.
Saga Y, Takeda H (2001) The making of the somite: molecular events in vertebrate segmentation. Nat Rev Genet 2(11): 835-845.
van Eeden FJ, Granato M, Schach U, Brand M, Furutani-Seiki M, et al. (1996) Mutations affecting somite formation and patterning in the zebrafish, Danio rerio. Development 123: 153-64.
Whittock NV, Ellard S, Duncan J, de Die-Smulders CE, Vles JS, Turnpenny PD (2004) Pseudodominant inheritance of spondylocostal dysostosis type 1 caused by two familial delta-like 3 mutations. Clin Genet 66(1): 67-72.



 A Harvardon dolgozó
A Harvardon dolgozó 


 Mielőtt azonban beleásnánk magunkat a PSM molekuláris rejtelmeibe, egy kis kitérőt teszek, hogy nagyvonalakban felvázoljam, miként tanulmányoznak a biológusok egy olyan komplex folyamatot mint a szomatogenezis.
Mielőtt azonban beleásnánk magunkat a PSM molekuláris rejtelmeibe, egy kis kitérőt teszek, hogy nagyvonalakban felvázoljam, miként tanulmányoznak a biológusok egy olyan komplex folyamatot mint a szomatogenezis.
 Ez az útvonal egyébként a gerincesekben univerzálisan fontos szereppel bír a szegmentáció kialakulásában (a mikéntről lásd egy picit alább). Mi sem mutatja ezt talán jobban, mint hogy számos olyan emberi betegség esetében, ahol az egyik tünet a gerincoszlop abnormális alakjában nyilvánul meg, a hibás génről kiderült, hogy valamit a Notch útvonallal kavar.
Ez az útvonal egyébként a gerincesekben univerzálisan fontos szereppel bír a szegmentáció kialakulásában (a mikéntről lásd egy picit alább). Mi sem mutatja ezt talán jobban, mint hogy számos olyan emberi betegség esetében, ahol az egyik tünet a gerincoszlop abnormális alakjában nyilvánul meg, a hibás génről kiderült, hogy valamit a Notch útvonallal kavar.

 A kígyók a két megoldás ötvözetét használják, bár a hangsúly az nagyon is az utóbbin van. A csirkék 16 és az egerek 13 db. sejtosztódásával szemben a kígyó PSM 21 sejtosztódáson megy keresztül. Szignifikáns különbség, de koránt sem akkora, hogy a nagyságrendnyi különbségért felelős lehessen. Sokkal inkább alkalmas erre a négyszer gyorsabban ketyegő sejtóra. Ez természetesen négyszer gyorsabb hullámokat idéz elő, amelyek így, egységnyi fejlődési idő alatt (vagyis más szervek fejlődéséhez viszonyítva), négyszer annyi szomitát hoznak létre, mint a rövid testű gerincesek, pl. zebrahalak – bár így a szomiták mérete lesz kezdetben kicsi.
A kígyók a két megoldás ötvözetét használják, bár a hangsúly az nagyon is az utóbbin van. A csirkék 16 és az egerek 13 db. sejtosztódásával szemben a kígyó PSM 21 sejtosztódáson megy keresztül. Szignifikáns különbség, de koránt sem akkora, hogy a nagyságrendnyi különbségért felelős lehessen. Sokkal inkább alkalmas erre a négyszer gyorsabban ketyegő sejtóra. Ez természetesen négyszer gyorsabb hullámokat idéz elő, amelyek így, egységnyi fejlődési idő alatt (vagyis más szervek fejlődéséhez viszonyítva), négyszer annyi szomitát hoznak létre, mint a rövid testű gerincesek, pl. zebrahalak – bár így a szomiták mérete lesz kezdetben kicsi.