
Kb. Szkeptikusékkal egyidőben figyeltem fel, a világ leghatásosabb kacsamájkivonatára, az Oscillococcinumra és egy picit meglepődtem.


Kb. Szkeptikusékkal egyidőben figyeltem fel, a világ leghatásosabb kacsamájkivonatára, az Oscillococcinumra és egy picit meglepődtem.
 Régóta lóg a levegőben a korábbi ígéretem, hogy kicsit behatóbban is foglalkozunk az aktuális influenza vírussal és azt hiszem a mostani hisztériánál keresve sem lehetne jobb időzítést találni.
Régóta lóg a levegőben a korábbi ígéretem, hogy kicsit behatóbban is foglalkozunk az aktuális influenza vírussal és azt hiszem a mostani hisztériánál keresve sem lehetne jobb időzítést találni.
Természetesen egy sorban is el lehetne intézni, hogy most akkor veszélyes-e a vírus, vagy sem, kell oltani, vagy sem, de mivel e legtöbb félreértés érzésem szerint abból ered, hogy sokaknak fogalmuk sincs miről beszélnek, egy kicsit mélyebben elmerülünk a témában. Végigvesszük, hogy akkor most pontosan hogyan is néz ki az influenza vírus, miképpen működik, mit tudunk a patomechanizmusáról a korábbi nagy influenzajárványok alapján. Miért kellhet az oltás, kell-e félni tőle, sőt még abba is megpróbálok belemenni, hogy miért hatékonytalan az oltás körüli kommunikáció és miért nem triviális ezen változtatni.
 Minden új, ígéretes technológia sajátos "hype" cikluson megy keresztül: először eltúlzott várakozások minimum világmegváltást remélnek tőle, majd amikor ez nem válik be keserű kiábrándulás jön és csak ezt követi a névértéken való kezelés. A génterápia a jelek szerint elért a harmadik ponthoz, bár a második szakasz talán sokkal keményebb lett, mint arra a technológia támogatói egykor számítottak.
Minden új, ígéretes technológia sajátos "hype" cikluson megy keresztül: először eltúlzott várakozások minimum világmegváltást remélnek tőle, majd amikor ez nem válik be keserű kiábrándulás jön és csak ezt követi a névértéken való kezelés. A génterápia a jelek szerint elért a harmadik ponthoz, bár a második szakasz talán sokkal keményebb lett, mint arra a technológia támogatói egykor számítottak.
A kezdetekben az eljárást leginkább halálos betegek utolsó mentsváraként alkalmazták: súlyos immunrendszeri zavarokban szenvedő gyerekekbe juttatták be a bennük hiányzó gén eredeti formáját, vírus alapú vektorok segítségével és reménykedtek, hogy helyreáll az immunműködésük. Tíz esetből nyolcban ez is történt, de a maradék két kis beteg a gyógyulásból hirtelen leukémiába esett, és mint kiderült szinte azonos okból: valahogy a retrovíruson bevitt immun gén egy vérképzésben fontos gén közelébe került, megzavart annak átíródását és ez vezetett az új megbetegedéshez.
 Mint azt két hete már beígértem, most az Ostrander laboratórium egyik legutóbbi eredményéről lesz szó, amiben a különböző kutya szőrtípusok genetikai eredetének erednek nyomába.
Mint azt két hete már beígértem, most az Ostrander laboratórium egyik legutóbbi eredményéről lesz szó, amiben a különböző kutya szőrtípusok genetikai eredetének erednek nyomába.
Kettős megközelítést használtak: egyrészt azt figyelték, hogy léteznek-e olyan genetikai markerek, amelyek hosszú szőrű/ drótszőrű/ pofaszakállás fajták egyedeiben szinte kivétel nélkül jelen vannak, míg más fajtákban nagyon ritkák. Másrészt kiemelten foglalkoztak egy olyan fajtával, ahol mindezen szőrzet jegyek egyaránt megfigyelhetők: a tacskókról van szó.
Az eredmények egyik érdekessége, hogy a legváltozatosabb fajok esetében ugyanazokat a mutációkat tudták az említett szőrzetjegyekért felelőssé tenni, a másik pedig az, hogy több, megvizsgált farkaspopulációból ezek a mutáns allélvariánsok egyaránt hiányoztak, vagyis a mutációk az ebszelídítés során alakultak ki, és nem pusztán már eredendően, egy ősi populációban meglevő genetikai sokszínűségről van szó, amelyből az emberi ízlés választott ki aztán valami neki tetszőt.
 A placebo hatás egyik legérdekesebb formája a fájdalomérzet csökkenése, olyan helyzetekben, amikor egyszerűen elhitetjük magunkkal, hogy ami történt nem is fáj, vagy ha fájt is, valamely (általában fiziológiásan irreleváns) cselekedetünk hatására a fájdalom minimalizálódott.
A placebo hatás egyik legérdekesebb formája a fájdalomérzet csökkenése, olyan helyzetekben, amikor egyszerűen elhitetjük magunkkal, hogy ami történt nem is fáj, vagy ha fájt is, valamely (általában fiziológiásan irreleváns) cselekedetünk hatására a fájdalom minimalizálódott.
Klasszikus példája ennek a szülői gyógypuszi, vagy amikor egyszerű, glicerines kenőccsel kezelnek fájó testrészeket, azt "fájdalomcsillapítóként" beharangozva.
Az igazi kérdés persze az, hogy miként is működik a placebo hatás? Miért nem érezzük a fájdalmat? Megszületik a fájdalomérzet, de a felsőbb agyi központokban valamiképpen felülíródik, vagy esetleg már az agyba el sem jut a fájdalomérzet?
Ezt tesztelendő, hamburgi kutatók egy csoportja mágneses rezonancia (fMRI) segítségével vizsgálta a placebo hatását testalanyok gerincoszlopában.
A paradigma egyszerű volt: azonos összetételű "fájdalomcsillapító" és "kontroll" krémet használva előbb kondicionálták a vizsgálati alanyokat: aki a "kontroll" kenőcsöt kapta az egy kifejezetten fájdalmas ingert kapott, míg a "fájdalomcsillapítós" csoport egy sokkal enyhébbet. (Ez fontos volt, hogy mindenki valóban elhiggye, a "fájdalomcsillapító" használ.) Ezt követően jött az igazi vizsgálat: a "különböző" kenőcsöket applikálva, egy köztes erősségű ingert használtak. Természetesen (ez ma már nem meglepő és nem is kérdés), a placebo jól működött, és akik azt hitték, hogy egy komoly analgézikus készítménnyel kenték be őket, szinte semmi fájdalmat nem éreztek, ellentétben a "kontroll" csoportos társaikkal. Ami figyelemreméltóvá tette a vizsgálatot az az, hogy a tipikus, fájdalom-specifikus gerincvelői aktivitás is eltűnt a placebo csoportban.
Vagyis ezekben az emberekben a fájdalomérzet soha nem is jutott el az agyig. Hogy pontosan miért nem, arról csak találgatni tudunk, de egy nagyon is jó okunk van feltételezni, hogy az ún. leszálló fájdalomgátló pályáknak kulcs szerepe van a folyamatban. Ezek az opiát típusú neurotranszmitterekkel "dolgozó" pályák klasszikusan arra szolgálnak, hogy különleges stressz helyzetekben (pl. ha harcolni kell, vagy menekülni) tompítsák a fájdalomérzetet. Úgy tűnik azonban, hogy az emberekben az (ön)szuggeszció képes a placebo hatás szolgálatába is állítani őket.
Eippert F, Finsterbusch J, Bingel U, Büchel C. (2009) Direct evidence for spinal cord involvement in placebo analgesia. Science 326: 404.
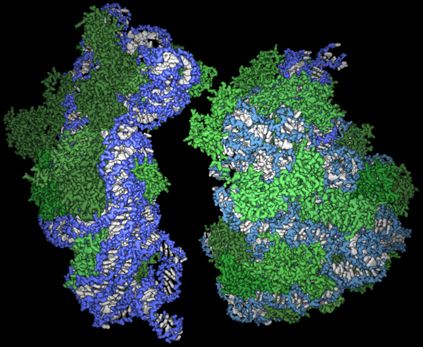 Rövidre fogva, a kémiai Nobelt idén a mellékelt ábrán látható gyönyörű és bonyolult struktúra feltárásáért ítélték oda (és ezzel immár sokadik éve, hogy ez a díj biokémiai jellegű felfedezésért lel gazdát).
Rövidre fogva, a kémiai Nobelt idén a mellékelt ábrán látható gyönyörű és bonyolult struktúra feltárásáért ítélték oda (és ezzel immár sokadik éve, hogy ez a díj biokémiai jellegű felfedezésért lel gazdát).
A három díjazott, Venkatraman Ramakrishnan, Thomas Steitz és Ada Yonath egyaránt sokat tett, hogy előbb a bakteriális, majd az eukarióta riboszómák struktúráját megismerjük, és ha van olyan felfedezés, amelyet rengeteg gyakorlati haszon követett, ez biztosan az.
A riboszomális 3D struktúra lehetővé tette, hogy rekonstruáljuk, miképpen is zajlik a fehérje szintézis, és közvetetten új távaltokat nyitott az antibiotikum kutatásban: hiszen a struktúra ismeretében célzottan lehet olyan molekulákat keresni, amelyek a prokarióta transzlációnak keresztbe tesznek, miközben az eukarióta megfelelőjét nem zavarják.
(A felhasznált ábra az Explore Origins oldalról származik.)
 (primavis kollega vendégposztja következik)
(primavis kollega vendégposztja következik)
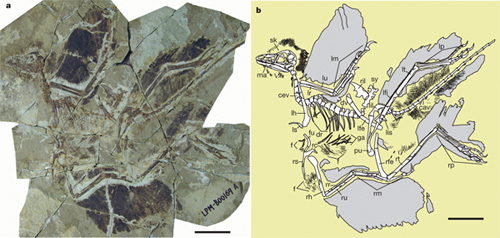
Az ÉK- Kinában található
Liaoning tartomány tollas dinoszauru-szokról már világszerte
ismert mezozoikumi lelőhelyei újabb „csodalényt” szolgáltattak. Ráadásul ez jóval idősebb is
az eddigi leleteknél, hiszen korát 155-159 millió évre becsülik.
 A humán paleontológiában nem ritka, hogy egy régi lelet nagy port kavar fel, de ezúttal nemcsak a fosszília kora az, ami miatt a felfedezés „réginek” minősíthető, hanem konkrétan előásásának pillanata is. Tim White és csapata 17 éve bukkant az Ardipithecus ramidus maradványaira, és néhány egész rövid publikációtól eltekintve, azóta is kvázi rejtegetik a világ szeme elől, hogy megfelelően tanulmányozhassák (jó munkához idő kell, ugye). CT rekonstrukció, izotópos vizsgálat, anyám tyúkja – mindent csináltak vele kb., amit elképzelni lehet. Most azonban lehull a fátyol „Ardiról”: a mai Science nem kevesebb mint 11 cikkben foglalkozik a hominid őssel és egykori életterével, és külön weboldalt szentel a témának.
A humán paleontológiában nem ritka, hogy egy régi lelet nagy port kavar fel, de ezúttal nemcsak a fosszília kora az, ami miatt a felfedezés „réginek” minősíthető, hanem konkrétan előásásának pillanata is. Tim White és csapata 17 éve bukkant az Ardipithecus ramidus maradványaira, és néhány egész rövid publikációtól eltekintve, azóta is kvázi rejtegetik a világ szeme elől, hogy megfelelően tanulmányozhassák (jó munkához idő kell, ugye). CT rekonstrukció, izotópos vizsgálat, anyám tyúkja – mindent csináltak vele kb., amit elképzelni lehet. Most azonban lehull a fátyol „Ardiról”: a mai Science nem kevesebb mint 11 cikkben foglalkozik a hominid őssel és egykori életterével, és külön weboldalt szentel a témának.
Ardi 4.4 millió éve élt, ami azt jelenti, hogy a lelet kb. 1 millió évvel idősebb, mint Lucy és a „korkülönbség” a jellegek szintjén is fellelhető. Lucy lábainak felépítése annyiban nagyon „emberi” volt, hogy nagy lábujjukat már nem tudták szembefordítani a talpukkal, ellentétben a ma élő csimpánz fajokkal. Ardi esetében azonban ez még nem figyelhető meg.