Amikor világot látott szűk másfél éve a kutya genom már írtam, hogy a kutyatenyésztés tekinthető akár az emberiség egyik legrégebbi és egyben leglátványosabb genetikai kísérletének is. Az elmúlt néhány ezer év alatt létrehozott fajták formagazdasága egészen lenyűgöző, és elsőrangú példája annak, hogy mi mindenre képes a(z ez esetben mesterséges) szelekció.
Amikor világot látott szűk másfél éve a kutya genom már írtam, hogy a kutyatenyésztés tekinthető akár az emberiség egyik legrégebbi és egyben leglátványosabb genetikai kísérletének is. Az elmúlt néhány ezer év alatt létrehozott fajták formagazdasága egészen lenyűgöző, és elsőrangú példája annak, hogy mi mindenre képes a(z ez esetben mesterséges) szelekció.
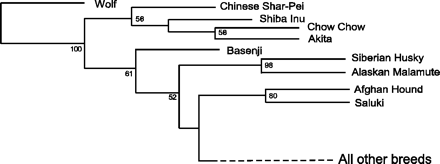
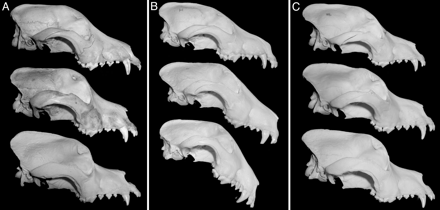
Egyes kutyafajták olyannyira különböznek egymástól, hogy ha például a csivavát és a dán dogot csak csontjaikról ismernénk, igen jó eséllyel két különböző, bár rokon fajnak tartanánk. A két eb között a méretkülönbség óriási, s ezzel el is érkeztünk a mai poszt kérdéséhez: mi lehet ennek az eltérésnek a genetikai oka?
A válaszhoz lehetne alkalmazni a tüskéspikók esetében is alkalmazott technikát, (keresztezzük a szóbanforgó tulajdonság két szélsőségét, majd az unokáikban elkezdjük a méretet és az egyes kromoszómális markereket együtt vizsgálni, hogy beazonosítsuk a tulajdonságért felelős DNS szakaszt), de egy palotapincsi és bernáthegyi keresztezése azért akadályokba ütközik (főleg a pincsi oldalán). Ilyen esetben érdemesebb szerényebb célokat kitűzni kezdetben, hiszen, mint azt látni fogjuk, az így szerzett tudás is remekül hasznosítható lesz.
A kutatók ez esetben kezdetben a portugál vízikutyára öszpontosítottak, azon a nem elhanyagolható okból kifolyólag, hogy ez a fajta igen nagy méretbeli változatosságot mutat. A kis- és nagyméretű vízikutyák genetikai markereit összevetve, a 15. kromoszóma egy rövidke szakasza tűnt ki: az itt elhelyezkedő markerek egy jól meghatározható csoportja minden egyes kisebb ebben jelen volt, de gyakran hiányzott a nagyobb méretűekből. A szóbanforgó szakasz egy növekedési faktort, az insulin-like growth factor 1-t (IGF1) kódol, s ez a gén egyben igen logikus jelölt is a méretbeli különbségek okozására: az IGF1 nemműködő verzióját hordozó egerek (és emberek) lényegesen kisebbek mint normális társaik. A vízikutyák esetében azonban a “kis” allél is működőképes IGF1 fehérjét hoz létre, csak lényegesen kevesebbet, mint a “nagy”, magyarán egy tipikus szabályozó-régió mutációval állunk szemben.
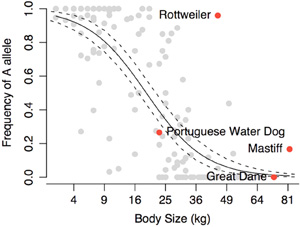 Persze kérdés, hogy mennyiben alkalmazható az egyetlen fajtából szerzett tudás a többiekre. Lehet, hogy a lecsökkent IGF1 szint más, aprónövésű fajtákban is fontos, de az is lehet, hogy azok egyéb okok miatt maradnak kicsik. A kérdést eldöntendő 143 kutyafajtát genotipizált végig a kutatócsoport és az eredmények szerint, a portugál vízikutyában talált “kis” IGF1 allél jelenléte ill. hiánya igen-igen jól korrelál a testmérettel. Jól, de nem tökéletesen (pl. a rottweilerek nagy többségében ez az allél van és mégsem kicsik), éppen ezért helytelen lenne az IGF1-t kinevezni A “méret-génnek”. Mint minden komplex, sok árnyalattal jellemezhető tulajdonság, a testméret is sok géntől függ (azaz poligénes). Az azonban bizonyosnak tűnik, hogy ez közül az egyik kiemelkedően fontos, az IGF1.
Persze kérdés, hogy mennyiben alkalmazható az egyetlen fajtából szerzett tudás a többiekre. Lehet, hogy a lecsökkent IGF1 szint más, aprónövésű fajtákban is fontos, de az is lehet, hogy azok egyéb okok miatt maradnak kicsik. A kérdést eldöntendő 143 kutyafajtát genotipizált végig a kutatócsoport és az eredmények szerint, a portugál vízikutyában talált “kis” IGF1 allél jelenléte ill. hiánya igen-igen jól korrelál a testmérettel. Jól, de nem tökéletesen (pl. a rottweilerek nagy többségében ez az allél van és mégsem kicsik), éppen ezért helytelen lenne az IGF1-t kinevezni A “méret-génnek”. Mint minden komplex, sok árnyalattal jellemezhető tulajdonság, a testméret is sok géntől függ (azaz poligénes). Az azonban bizonyosnak tűnik, hogy ez közül az egyik kiemelkedően fontos, az IGF1.
Sutter, NB, Bustamante, CD, Chase, K, Gray, MM, Zhao, K, et al. (2007) A single IGF1 allele is a major determinant of small size in dogs. Science 316: 112-115.

 Ha rákos daganatok, azaz rosszindulatú tumorok kerülnek szóba, akkor hajlamosak vagyunk szinte kizárólag csak olyan sejtvonalakra gondolni, amelyek adott szervezeten belül ilyen-olyan módon összeszednek bizonyos mutációkat, amelyek aztán lehetővé teszik, hogy gátlás nélkül osztódjanak, kapillárisokat édesgessenek magukhoz (hogy így tápanyagokhoz jussanak) és ide-oda vándoroljanak a véráramba, más szövetekben áttéteket hozva létre. Az általános képbe azonban nem tartozik bele, hogy a dagantos sejteket, mint egy ragályos betegség ágenseit lássuk, amelyek parazitaként más egyedekre is képesek átterjedni. Pedig léteznek ilyen rákos megbetegedések (ha nem is túl sok), egyik pl. az ebekben Sticker szarkómaként ismert kór.
Ha rákos daganatok, azaz rosszindulatú tumorok kerülnek szóba, akkor hajlamosak vagyunk szinte kizárólag csak olyan sejtvonalakra gondolni, amelyek adott szervezeten belül ilyen-olyan módon összeszednek bizonyos mutációkat, amelyek aztán lehetővé teszik, hogy gátlás nélkül osztódjanak, kapillárisokat édesgessenek magukhoz (hogy így tápanyagokhoz jussanak) és ide-oda vándoroljanak a véráramba, más szövetekben áttéteket hozva létre. Az általános képbe azonban nem tartozik bele, hogy a dagantos sejteket, mint egy ragályos betegség ágenseit lássuk, amelyek parazitaként más egyedekre is képesek átterjedni. Pedig léteznek ilyen rákos megbetegedések (ha nem is túl sok), egyik pl. az ebekben Sticker szarkómaként ismert kór.