Már elég sokat írtunk a MucoRice platformról, de még mindig nem elég, nagyon úgy tűnik, hogy egy eléggé széles körben használható és kifejezetten sokoldalú fehérjetermelő rendszert sikerült kifejleszteni a japánoknak. Az alapja annyi, hogy gátolják a rizsszemben legnagyobb mennyiségben termelődő két fehérjét kódoló gén kifejeződését, helyette a kívülről bejuttatott transzgének által kódolt fehérjék termelődnek a rizsszemben. Ennek a módszernek előnye a nagy kitermelés, hiszen a MucoRice rizzsel semmit sem kell csinálni, csak vetni-aratni, ahogy minden más rizst is, ráadásul a jelek szerint a rizs legalább egy évig eláll minden különösebb tárolás nélkül, nyilván ez elmondhatatlan előny bármilyen más rekombináns fehérjetermelő rendszerhez képest. Ráadásul a termelt fehérje kinyeréséhez egyszerűen csak meg kell őrölni a rizst és sós vízbe áztatni, hogy a termelt rekombináns fehérje oldatba kerüljön.
Ha a ma ismertetett módszer úgy működik, ahogyan a szerzők állítják, alighanem éppen most sikerült forradalmasítani a gyógyszergyártást. A gyógyszeripar legújabb aranytojást tojó tyúkjai ugyanis a monoklonális ellenanyagok, röviden ezek egy-egy immunglobulin molekula tömegei, amelyek egy adott epitópot ismernek föl. A gyógyászatban a jelentőségük óriási, mivel egy embernek egyszerűen injekcióban beadható egy nagy adag emberi eredetű ellenanyag, amely a vérben keringve megtalálja az általa felismert fehérjét és hozzákötődve gátolja annak a működését. Ráadásul mivel szédítően sok különböző ellenanyag lehetséges, elméletileg akármelyik fehérjét felismerő monoklonális ellenanyag előállítható, vagyis szédítően sok különböző betegségre jelenthet megoldást egy-egy ellenanyag. Ráadásul a tapasztalatok alapján a mellékhatások elhanyagolhatóak, mivel az ellenanyag fehérjetermészetű, egyszerűen a többi fehérjével együtt a sejtek előbb-utóbb megemésztik, nincsenek mérgező melléktermékeik.
Az előnyei mellet a hátrányairól is szót kell ejteni, az első nyilván abból következik, hogy ilyen specifikusak, egy ellenanyag egyetlen fehérjét ismer föl, ha esetleg két-három célpontra akarunk hatni, akkor bizony két-károm különböző ellenanyagot kellene adagolni. A másik hátrányuk az ár, ugyanis eddig monoklonális ellenanyagokat csak sejtvonalakban tudtunk termeltetni, ennek megfelelően a termeltetésük majd a tisztításuk pofátlanul sokba került, mondjuk egy beteg infliximab kezelése évente tizenötezer dollárba kerül, vagyis több mint hárommillió forintba, nyilván erre azért kevés embernek telik, akármilyen hatékonyak is ezek a szerek.
No de mit csináltak a mai cikk szerzői Michiyo Abe és munkatársai? Gondoltak egyet, hogyha a monoklonális ellenanyagokkal épp az a gond, hogy drága őket előállítani, nekünk meg épp van egy hihetetlen olcsó fehérjetermelő rendszerünk, miért ne próbáljunk meg a MucoRice -ban ellenanyagokat termelni? A TNF molekula bejáratott célmolekula különböző autoimmun kórképek például reuma és Crohn-betegség esetén is, több TNF gátló monoklonális ellenyanyag is hozzáférhető a piacon. Már korábban mások leírtak az emberi és az egér TNF molekulát felismerő két láma ellenanyagot, így egyszerűen csak fogták az egér TNF -et felismerő fehérjét kódoló gént és bevitték a már jól kitaposott MucoRice rendszerükbe, ez lett a MucoRice-mTNF-VHH. Ellenőrizték, nagyon szépen termelte a rizsük a rekombináns fehérjét, a rizsszemekben gramonként átlagosan 14,5 mg mTNF-VHH -t mértek, ami nagyon jó hatásfokkal ki is oldódott a rizslisztből ha foszfátpufferelt sóoldatban áztatták, amiből a rekombináns fehérje gélfiltrálással, egy filléres tisztítási eljárással nagy hatékonysággal kinyerhető. Példaként hozzák, hogy 25 g MucoRice-mTNF-VHH porból 300 mg rekombináns fehérjét nyertek ki.
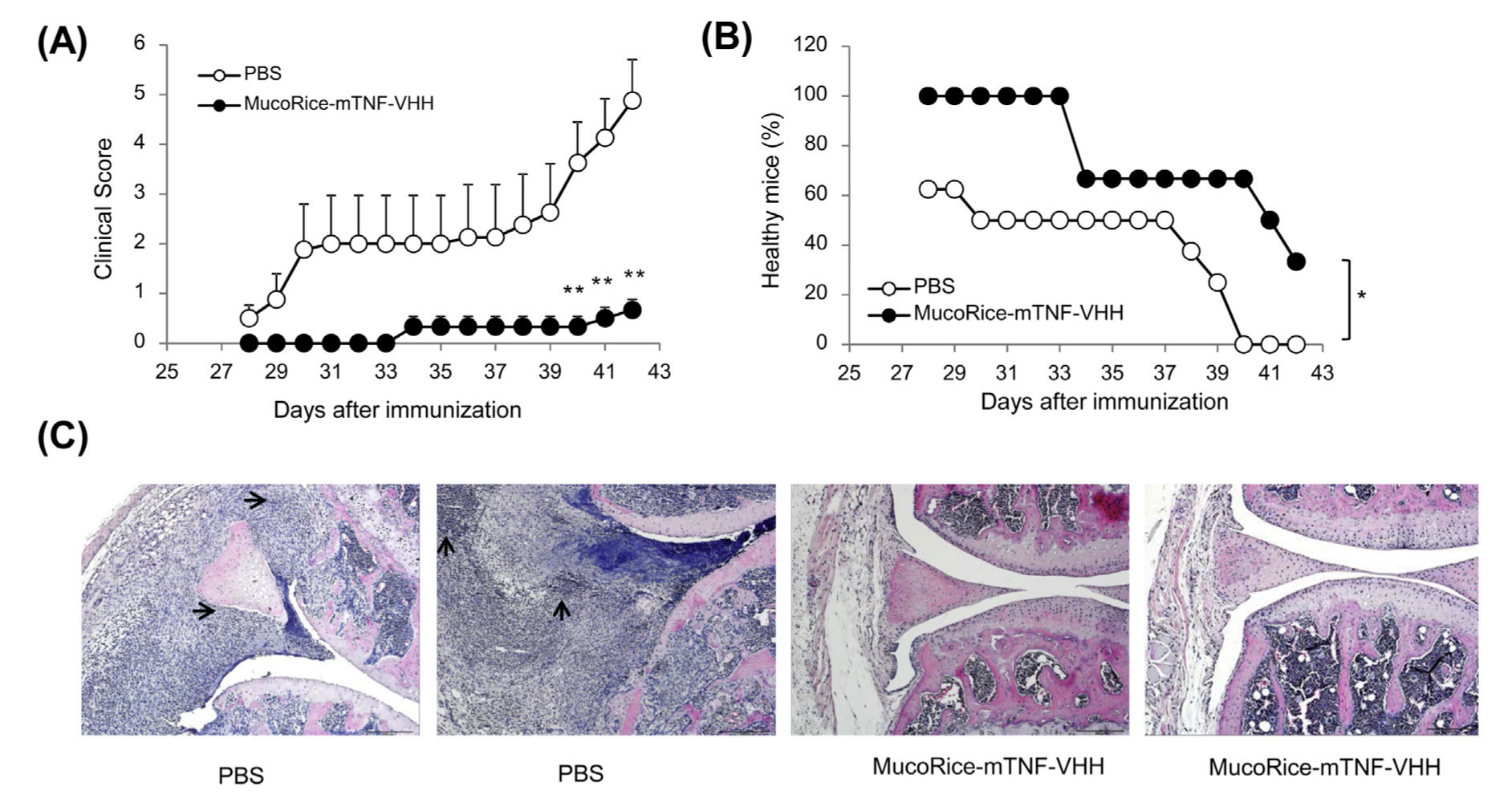
Ezek után fogták a reuma egér modelljét, amit ezek szerint CIA-indukált egereknek hívnak, ezekbe marha kollagént oltanak Freund adjuvánssal, így váltják ki bennük az autoimmun betegséget, amikor az immunrendszer megtámadja a szervezet saját szöveteit. Ezeknek az egereknek elég durva reumájuk alakul ki, de mint ahogy a második „A” ábrán látható, a MucoRice által termelt mTNF-VHH fehérje injekciók megvédték őket a reumától, a tüneteik egészen enyhék maradtak, a mancsaik nem dagadtak föl. Sőt, eleve kevesebb egér kapott reumát, az egészséges egerek arányát mutatja a „B” ábra. Ugyanez a különbség látszik a térdízületek keresztmetszeti képein is a „C” ábrán, az mTNF-VHH kezelt egerek térdei kevésbé gyulladtak, mint a kezeletleneké.
Magyarul ha ez az ellenanyagfragment az emberben is úgy működik, mint az egérben, alighanem a szerzőknek sikerült forradalmasítani a gyógyszeripart, nyilván egy csomó más ellenanyag ugyanígy olcsón megtermeltethető lenne ebben a rizsben, márpedig ezen a piacon minden árcsökkenés érezhetően közelebb hozza a betegekhez a gyógyszereket. Egészen pontosan forradalmasítaná, ha hagynánk, mert ugye jelenleg ez a beavatkozás génmódosításnak minősül, a terméke GMO és mint ilyen, tilos is vetni a Föld jelentős részén.
Abe, M., Yuki, Y., Kurokawa, S., Mejima, M., Kuroda, M., Park, E. J., … & Kiyono, H. (2014). A rice-based soluble form of a murine TNF-specific llama variable domain of heavy-chain antibody suppresses collagen-induced arthritis in mice. Journal of Biotechnology, 175, 45-52.
