 Napjaink alulértékelt, de komolyan veendő problémáinak egyike az antibiotikumrezisztens bakteriális kórokozók terjedése. A Távol-Keleten lappangó madárinfluenza variánsokkal egyetemben, ezeknek van a legnagyobb esélye arra, hogy globális káoszt okozzanak.
Napjaink alulértékelt, de komolyan veendő problémáinak egyike az antibiotikumrezisztens bakteriális kórokozók terjedése. A Távol-Keleten lappangó madárinfluenza variánsokkal egyetemben, ezeknek van a legnagyobb esélye arra, hogy globális káoszt okozzanak.
A probléma persze nem teljesen váratlan, sőt ha jobban megnézzük kialakulásában igen jelentős és jól dokumentált szerepet játszottunk mi magunk, emberek is.
Az egyes antibiotikumokkal szembeni rezisztencia ugyanis minden esetben szabványos természetes szelekcióval alakult ki: az alkalmazásukkal egyetemben szelekciós nyomás alakult ki a bakteriális célpopuláción, amelynek eredményeképpen a „célcsoport” vagy elpusztult (szerencsére ez volt a gyakoribb), vagy egy-két mutáns „hírvivő” révén fennmaradt. Ez azzal magyarázható, hogy az antibiotikum kezeléssel párhuzamosan természetesen a baktériumok a szervezetben tovább osztódtak, és minden egyes osztódás során bizonyos valószínűséggel mutációkat szedhettek össze. Ha megfelelő mutáció jön létre, akkor a baci kikerüli az antibiotikumok hatását, rezisztensé válik és vidáman osztódik tovább.
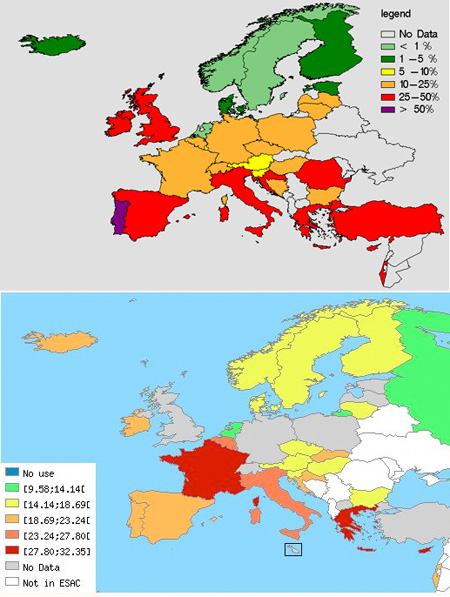 Mivel sok beteget kezelnek antibiotikummal, ráadásul minden betegben milliószámra hemzsegnek a bacik, a nagy számok törvénye alapján előbb-utóbb biztos lesz alkalom a megfelelő mutáció megjelenésére. Sőt ebből a kis szabályból az is levezethető könnyen, hogy minél elterjedtebb az antibiotikumhasználat, annál gyorsabb lesz a rezisztencia kialakulása. (Megspékelve mindezt azzal, hogy a baktériumok képesek kisebb DNS darabokat ún. „horizontális géntranszferrel” is terjeszteni, igazából sejthető, hogy a baktériumok számára hasznos mutációk tűzvész gyorsaságával képesek elterjedni.) Ez pedig nemcsak elméleti szépelgés, hanem olyasmi, amit alátámaszt az empirikus megfigyelés is: ha összevetjük a European Antimicrobial Resistance Surveillance System (EARSS) keretén belül gyűjtött adatokat a European Surveillance of Antimicrobial Consumption (ESAC) felméréssel, az összefüggés, ha nem is tökéletes, de szembetűnő.
Mivel sok beteget kezelnek antibiotikummal, ráadásul minden betegben milliószámra hemzsegnek a bacik, a nagy számok törvénye alapján előbb-utóbb biztos lesz alkalom a megfelelő mutáció megjelenésére. Sőt ebből a kis szabályból az is levezethető könnyen, hogy minél elterjedtebb az antibiotikumhasználat, annál gyorsabb lesz a rezisztencia kialakulása. (Megspékelve mindezt azzal, hogy a baktériumok képesek kisebb DNS darabokat ún. „horizontális géntranszferrel” is terjeszteni, igazából sejthető, hogy a baktériumok számára hasznos mutációk tűzvész gyorsaságával képesek elterjedni.) Ez pedig nemcsak elméleti szépelgés, hanem olyasmi, amit alátámaszt az empirikus megfigyelés is: ha összevetjük a European Antimicrobial Resistance Surveillance System (EARSS) keretén belül gyűjtött adatokat a European Surveillance of Antimicrobial Consumption (ESAC) felméréssel, az összefüggés, ha nem is tökéletes, de szembetűnő.
Mindenesetre a napokban újabb érvvel gazdagodtak azok, akik a nyakló nélküli antibiotikumfogyasztás ellen kampányolnak: egy új tanulmány azt mutatta ki, hogy a szubletális (vagyis az elpusztításhoz szükségesnél kisebb dózisban) adagolt antibiotikum, megnöveli a rezisztencia kialakulását – ráadásul nem egyszerűen azért, mert szelekció van.
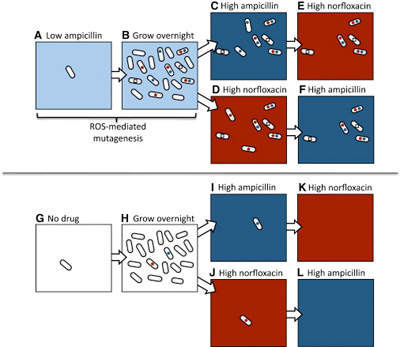 Az antibiotikumok hatásmechanizmusának egyik utolsó lépése általában ún. reaktív oxigénszármazékok (ROS) segítségével zajlik: ezek – mint nevük is mutatja – nagy valószínűséggel reakcióba lépnek a környékükön levő molekulákkal (cukrokkal, fehérjékkel, nukleinsavakkal egyaránt), azokat működésképtelenné téve. Most azonban kiderült, hogy a sejtekben megjelenő ROSok mennyisége arányos az alkalmazott antibiotikumok arányával, vagyis szubletális dózisnál is felszabadul belőlük egy kis mennyiség. Ez ahhoz kevés, hogy a sejtet elpusztítsa, ahhoz viszont elég, hogy a DNS-ben hibákat hozzon létre, vagyis megnövelje a mutációk számát, az ún. mutációs rátát.
Az antibiotikumok hatásmechanizmusának egyik utolsó lépése általában ún. reaktív oxigénszármazékok (ROS) segítségével zajlik: ezek – mint nevük is mutatja – nagy valószínűséggel reakcióba lépnek a környékükön levő molekulákkal (cukrokkal, fehérjékkel, nukleinsavakkal egyaránt), azokat működésképtelenné téve. Most azonban kiderült, hogy a sejtekben megjelenő ROSok mennyisége arányos az alkalmazott antibiotikumok arányával, vagyis szubletális dózisnál is felszabadul belőlük egy kis mennyiség. Ez ahhoz kevés, hogy a sejtet elpusztítsa, ahhoz viszont elég, hogy a DNS-ben hibákat hozzon létre, vagyis megnövelje a mutációk számát, az ún. mutációs rátát.
És mivel a mutációk „vakon” születnek, az alacsony dózisban alkalmazott ampicillin ugyanakkora eséllyel hoz létre ampicillin-rezisztenciát, mint norfloxacin-rezisztenciát, hiába van teljesen más molekulacsaládokról szó.
Kaufmann BB, Hung DT (2010) The Fast Track to Multidrug Resistance Molecular Cell 37(3): 297-298.
Kohanski MA, DePrsito MA, Collins JJ (2010) Sublethal Antibiotic Treatment Leads to Multidrug Resistance via Radical-Induced Mutagenesis Molecular Cell 37(3): 311-320.

Mégis, akkor mi a megoldás? 😉
Én tudom, mi a megoldás:
Apró cukorgolyók, azok meggyógyítanak mindent, mellékhatás nélkül. Különösen segít, ha mágnesekkel veszed magad körlül, miközben polarizált fény éri a testedet.
Hogy komolyra fordítsam a szót, szerintem ez egy örök harc a külömböző antibiotikumok és a baktériumok között. Ki kell fejleszteni egy újat, majd ha arra is rezisztens lesz, akkor még újabbat, és így tobább. Sajnos limitáltak az ismereteim de szerintem ha létezne legalább 4-5 féle hatóanyagú antibiotikum, akkor az egyikre csak nem immúnis.
@Meister:
1. Antibiotikumot csak receptre.
Önmagától a jónép tonnaszám szedi be, össze-vissza, ráadásul nem is csak baktériumos fertőzésekre. Minden fölöslegesen beszedett pirula egy újabb esély arra, hogy valamelyik baciban kialakuljon a rezisztancia.
2. Antibiotikumot csak akkor, ha tudjuk, mi okozza a fertőzést.
Magyarországon az orvosok gyakran úgy „kezelik” a kuncsaftot, hogy van egy listájuk, amiről fölirják az első antibiotikumot, „Jöjjön vissza két hét múlva” ha nem javul, fölirják a másodikat, ha akkor sem, a harmadikat, stb. Ez hülyeség. Csak akkor szabadna elkezdeni a kezelést, ha tudjuk, mit kezelünk, milyen élőlényt akarunk irtani, találomra tilos.
3. A kórházakba több takarítónőt.
A kórházakban tenyésznek elsősorban a mindenre ellenálló bacik, a kórházi fertőzések elsődleges oka pedig az, hogy a takarításon spórolnak, így némelyik kórház olyan mocskos, hogy vágóhídként sem kapna működési engedélyt. (Tudom, miről beszélek, műtöttek már ilyen helyen.) Akármire rezisztens egy baktérium, a hipó megöli (75 ft/liter) míg ha már sikeresen bejutott a szervezetedbe csak a legdurvább antibiotikumokkal irtható (20-60.000 ft/doboz).
4. Minden kúrát végigszedni.
Ha az orvos felír egy doboz antibiotikumot, azt végig be kell szedni. Ha abbahagyod, amikor megszűnnek a tünetek, még nem pusztult el az összes baci, néhány töredékszázaléka túlél, őbelőlük alakulnak ki a rezisztens törzsek.
Ha ezeket a szabályokat kőkeményen betartanák, azzal lassítani lehetne a rezisztens törzsek kialakulását. Megállítani nem, mert erről szól az evolúció, ha egy élőlény szelekciós nyomás alá kerül, alkalmazkodik hozzá.
@SexComb:
„2. Antibiotikumot csak akkor, ha tudjuk, mi okozza a fertőzést.”
Sajnos nem minden esetben van idő megvárni a tenyésztés eredményét. Ha súlyos állapotban kerül a beteg az orvoshoz, akkor egy széles spektrumú antibiotikum sokat segíthet, ha bakteriális fertőzésre gyanakszunk.
@SexComb:
Köszi.
Egyedül a 2-es pontot nem értem. Ez azt jelenti, hogy ha 38 fokos lázzal elbattyogok a háziorvosomhoz, akkor neki nem szabadna felírnia antibiotikumot, míg nem csinált köpetminta-tenyésztést?
A többi pontodban írtakkal egyetértek, és én mindig végig is szedem, amit kapok. (Bár az esetek nagy részében nem ér semmit, és a dokim nem is ír fel túl gyakran antibiotikumot.)
@Meister:
Elvileg. Gyakorlatilag van rá mód, hogy valamilyen alap-szinten a kétfajta fertőzést elkülönítsék. Angliában egyébként rohadtul nem szeretnek felírni antibiotikumot; amikor egyszer ottéltemben elkaptam valami nyavalyát és már három napja nyelni alig bírtam, akkor szabályosan ki kellett könyörögjem egy kis indiai dokiból a receptet (ami egyébként aztán elég gyosan hatott is).
Van ez az X ceg Y termeke, amely „Bacillus clausii” sporat tartalmaz, fiolankent 2 milliard darabot. Naponta 2-3 amulla, azaz 4-6 milliard bakterium naponta. Mindegyike „tobbszorosen” antibiotikum rezisztens a leiras szerint.
Azt irja „Antibiotikum kezeles ideje alatt a keszitmeny bevetele az antibiotikum ket adagjanak bevetele kozotti idoszakban tortenjen.” szoval lehet szedni antibiotikummal. Mennyire feljek attol, hogy ezen bakteriumok tobbszorosen antibiotikum rezisztens genjei horizontalis gentranszferrel a betegseget okozo bakteriumokba jutnak?
Én magamtól vagyok úgy, hogy csak akkor megyek dokihoz, ha tényleg döglődök. Nyelni nemtudás és 38 fokos láz nem ez a kategória, az magától is gyorsan elmúlik.
Egyébként nem egészen tiszta (nem kötekedésből, igaziból nem tiszta), hogy a dokinak miért is kell felírni azonnal az antibiotikumot… hogy ne fertőzz meg másokat? Hogy nőjön a GDP, hamarabb munkába állj?
@el.cid
@Meister
Nem is arra vonatkozik ez az eset, amikor halni készülsz, a „jöjjön vissza két hét múlva” kitételből is látszik. Olyankor úgyis napokon belül dűlőre viszik a dolgot (meghalsz vagy meggyógyulsz).
Ebből a szempontból az igazán veszélyesek az elhúzódó fertőzések, például ha elmész a körzeti orvosodhoz azzal, hogy csíp a vizeleted, felír egy doboz C*fran -t, oszt menj Isten hírivel. Nem leszel jobban, visszajössz két hét múlva, kapsz egy doboz Augmentint, gyere vissza két hét múlva. Ha visszajössz, eltelt egy hónap, már esetleg elküldenek egy vizeletmintát tenyésztésre, hogy mégis mi bajod lehet, ami nyilván tök negatívan jön vissza, mert már egy hónapja antibiotikumot szedsz, az eredeti kórokozók egy részét már elölte az eddigi kezelés, de a maradék vígan tenyészik. Nem szólva arról, hogy gy csomó baktérium nem is tenyészik a szokásos táptalajon, azok kimutatására esély sincs.
Ilyenkor a szervezetedben, vagy éppen a felületén élő összes többi baktérium négy hete gyógyszerben ázik, teljesen fölöslegesen, tökéletes terep ez ahhoz, hogy létrejöjjenek ezek a csodabaktériumok. Sajnos ez az eljárás gyakoribb, mint gondolnánk, egy csomó embert így kezelnek.
Hahh, anyósom úgy októbertől januárig szenvedett tüdőgyulladásban. Kapott valamicske antibiót, keveset, jobban lett, majd megint lázas, megint antibió, és így eljátszottak az orvossal… Most már jól van. Röhej. Láttam valamelyik todományos csatornán egy műsort, ahol több országban megpróbáltak szerezni antibiotikumot, és a legtöbb helyen annyi az egész, hogy bemész a gyógyszertárba, közlöd, hogy folyik az orrod, adjanak valamit és adnak. Hát ez a szívás.
SexComb: Es az is biztos, hogy amig valami nagyobb katasztrofa nem lesz, nem fog valtozni semmi.
A H1N1 óta mindig olvasgatlak benneteket, valamihez egy kukkot sem értek, de van ami nagyon érdekel, például ez a téma is. Szindbád írta, a „jóbacilus” törzseket, amit antibiotikumok mellé szedetnek (itt még nem kötelezően, más országokban, nyugatra már 10-20 éve biztos). Csak egy kérdés merült fel bennem, ha pl a Bacillus Clausii antibiotikum rezisztens, akkor mi értelme van annak, hogy két antibiotikum bevétel között kell bevenni? Mellesleg én is így csinálom automatikusan, mert én meg nem gondoltam őket rezisztensnek.
De én hozzátok képest ehhez semmit sem értek, ezért a kérdés, ha valaki felvilágosítana, nagyon örülnék. Köszi. 🙂
(Csak mert a kisfiam négyévesen most kapott először antibiotikumot, és nem szeretném, ha ez ezentúl gyakori lenne nálunk, mindenesetre a téma eléggé érdekel.)
Elnézést, válaszolna valaki a 7. kérdésre? Most kétségek gyötörnek, hogy akkora hülyeséget kérdeztem, vagy egyszerűen nincs válasz?
@Szinbad:
Dehogy hülyeség, sőt. A gond az, hogy nem tudok konkrét számot, de szerintem értelemszerűen az esély nagyobb, mint nulla.
ÁÁÁ, Szindbád, itt aki hülyeséget kérdezett, az valószínűleg én voltam…. 🙂
Bár még mindig nem értem, hogy ha úgyis rezisztens, akkor miért nem lehet egyszerre bevenni a lactobacillusokat az antibiotikumokkal.
mynona: az, hogy rezisztens, nem azt jelenti, hogy barmilyen koncentracioban elviseli az antibiotikumot. Ha a gyogyszerrel egyutt veszed be, akkor a belcsatornaban olyan tomeny, magas helyi koncentracioju antibiotikummal talkozik, hogy karosodhat tole.
Ha az antibiotikum mar felszivodott, egyenletesen eloszlott a szervezetedben, azt mar kepes elviselni.
De jó, hogy válaszoltál, köszönöm szépen. 🙂