A Parkinson-kór egy progresszív, a központi idegrendszert érintő betegség, amelyet a köztudatban elsősorban állandó remegéssel és mozgáskoordinációs zavarokkal kapcsolunk össze. Erre utal a betegség kissé régies magyar elnevezése is, a „reszkető bénulás”. A közismert tünetek mellett azonban a betegeknek legalább ennyi szenvedést okoz a szorongás, az esetenként mély depresszió, alvási zavarok, a személyiségjegyek torzulása és a demencia, amelyek mind tipikus tüneteknek számítanak.
A Parkinson-kór pontos kiváltóokai alig ismertek, környezeti és genetikai faktorok egyaránt közrejátszhatnak kialakulásában. Ami a genetikát illeti eddig vagy egy tucat génről állapították meg, hogy mutációja nagyban hozzájárul a kórkép kialakulásához. Ezek egy jelentős része a lizoszómális rendszer működésével, a vezikuláris transzport folyamatokkal, illetve az autofágiával kapcsolatos szerepet tölt be. Mind közül a legfontosabb talán az SNCA gén, ami az alfa-synuclein nevű fehérjét kódolja. E fehérje felhalmozódása a kórlefolyás egy tipikus eleme.
Akármilyen sejtszintű, molekuláris folyamatok is vezetnek a betegség kialakulásához, a közvetlen ok jól ismert: a középagy egy meghatározott területén, az un. substantia nigra állományában a dopaminerg idegsejtek rohamos pusztulásnak indulnak. Ezek a sejtek az akaratlagos és a spontán mozgások szervezésében játszanak szerepet, így pusztulásuk magyarázatot szolgáltat a Parkinson-kór jellemző motoros tüneteire. Minthogy a neuronok elvesztése irreverzibilis, a betegséget gyógyíthatatlannak tekintik.
Az őssejtkutatás azonban e területen is nagy ígéreteket hordoz magában. A Kiotói Egyetem klinikáján 2017-ben hét páciens bevonásával vágtak bele egy merész vizsgálatba, amely során újraprogramozott sejteket injektálnak a betegek agyába, annak reményében, hogy azok beépülve képesek lesznek pótolni a substantia nigra elpusztult dopaminerg sejtjeit. A klinikai kísérletet végző orvosok reményei nem alaptalanok, a kísérletsorozat egyik vezetője, az őssejtbiológus Jun Takahashi kutatócsoportjával ugyanis korábban jávai makákókon (Macaca fascicularis) sikeresen végzett hasonló kezeléseket. A majmokat előzőleg egy MPTP-nek becézett neurotoxinnal (tisztességes nevén: 1-metil-4-fenil-1,2,3,6-tetrahidropiridin) kezelve Parkinson-kórt idéztek elő, majd humán indukált pluripotens őssejtekből (hiPSC) származó idegi őssejtekkel kezelték őket. Ezeket az idegi őssejteket úgy állították elő, hogy azok elvben csak olyan dopaminerg sejtek létrehozására legyenek képesek, mint amilyenek a substantia nugrában is vannak. A majmok agyát később szövettani technikákkal feldolgozva megállapították, hogy az őssejtek beépülnek a kívánt területre, valóban dopaminerg neuronokká differenciálódnak, és képesek kialakítani azokat az idegi kapcsolatokat, amelyeket egy tisztességes neuronnak a substantia nigrában ki kell alakítania (az alábbi ábra ezt szemlélteti). A beteg makákók tünetei enyhültek, továbbá fontos megállapítás volt, hogy (legalábbis a kezelést követő két évben) az őssejtekből nem fejlődött semmilyen tumoros elfajulás.
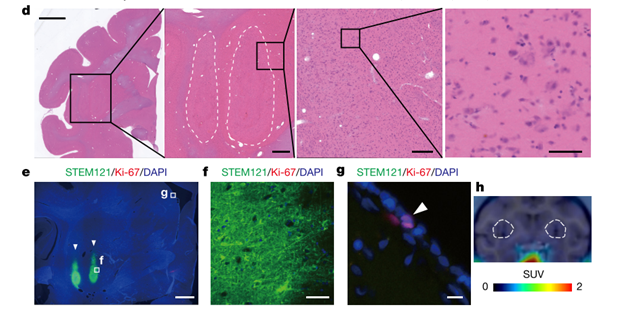
A fenti kisérleteken fellelkesülve az első pácienst 2018 októberében műtötte Takayuki Kikuchi sebészgárdája. A három órás beavatkozás során 2,4 millió idegi őssejtet ültettek be az 50-es éveiben járó férfi agyába, 12 jól definiált pozícióban. A sejtek egy anonim donorból származnak, átprogramozásukat a Kiotói egyetemen végezték, és a létrehozott sejtvonalat ott is tárolják. A beteg jól van, s ezeddig nem következett be semmilyen nemkívánt mellékhatás. Orvosai optimisták. A többi hat páciensen 2020-ig bezárólag tervezik a beavatkozás elvégzését.
Kíváncsian várjuk a fejleményeket.
Japán élenjárónak számít az őssejtalapú regeneratív orvoslásban. A világon először itt végeztek el eredményesnek nevezhető hiPSC alapú terápiát makula degenerációban szenvedő pácienseken, s jelenleg is több hasonló terápiás lehetőség áll fejlesztés alatt. A Japán kormány komoly forrásokkal támogatja az őssejtkutatást és a regenerációs medicínák fejlesztését, aminek egyik következménye (és azóta oka) a 2012‑ben kiosztott orvosi és fiziológiai Nobel-díj. Az ilyen természetű kutatások egy másik hajtóereje lehet, hogy az országban a szervtranszplantációk történeti és kulturális okokból kifolyólag szigorú szabályozás alatt állnak, így az alternatív lehetőségekre fokozott igény mutatkozik az egészségügy részéről.
Kikuchi T, Morizane A, Doi D, et al. (2017) Human iPS cell-derived dopaminergic neurons function in a primate Parkinson’s disease model. Nature 548(7669):592-596
https://www.nature.com/articles/d41586-018-07407-9
https://en.wikipedia.org/wiki/Organ_transplantation_in_Japan

Jó hír és ígéretes terápia a parkinson kórt okozó “néger szubsztancia” pótlása őssejttel. 🙂 Idétlen szójáték volt, nem rasszista szándékkal írtam.
Amit viszont laikusként nem értek ma sem. A gyíkocska ha elveszti a farkát, képes újranöveszteni (hogy végtag veszik el, vagy egy agyi szövet, gondolom végül is mindegy). Amit nem értek, minek ehhez őssejt, a gyík vagy a földi giliszta képes elveszett testrészeit újra növeszteni? Mi emberek, meg még sok másik lény miért nem? Minden testi sejtünkben benne van minden testi sejt helye, vagyis ha észleli egy a felkarom hogy hiányzik mellőle az alkarom mondjuk baleset miatt, ahogy képes összehegedni a seb és új bőr nőni a csonkolt felületen, ilyen erővel visszanőhetne az elveszett alsó kar is. Pontosabban minden infó a genomban minden testi sejtben benne van. Azt még értem hogy az őssejt nem specialista, ezért bármilyen szövetté képes alakulni. Amit nem értek, hogy a felkarom testi sejtjei az alkarom testi sejtjeivel azért elég közeli “szövet rokonok” lehetnek.
Boccs a pongyola fogalmazásért, remélem kérdésem értelme (ha volt neki :-O) átment. 🙂