 Az antibiotikumoknak ellenálló baktériumtörzsek megjelenése egyre komolyabb veszélyt jelent világszerte, köszönhetően az antibiotikumfejlesztés leállásának. Néhány baktériumtörzs ellen már tehetetlenek az orvosok, hiszen minden elérhető gyógyszernek ellenáll. Camilo Barbosa és munkatársai egy egészen szokatlan megoldást írtak le a Plos Biology lapban: Azt vizsgálták, mennyire hatékonyak a különböző antibiotikumok párosával alkalmazva. Az, hogy egyszerre két-három antibiotikummal kezeljünk egy fertőzést körülbelül azóta lebegő ötlet, amióta a második ilyen szert felfedezték, de ez a megoldás mégsem terjed el széles körben, egy-két nevezetes kivételtől eltekintve (malária, HIV, tuberkulózis) nem használják. Az akadálya az evolúció, a kórokozók folyamatosan evolválnak, ha már két hatóanyaggal szemben ellenállóak, hamar megjelennek a kettő ellen egyszerre ellenálló törzsek is.
Az antibiotikumoknak ellenálló baktériumtörzsek megjelenése egyre komolyabb veszélyt jelent világszerte, köszönhetően az antibiotikumfejlesztés leállásának. Néhány baktériumtörzs ellen már tehetetlenek az orvosok, hiszen minden elérhető gyógyszernek ellenáll. Camilo Barbosa és munkatársai egy egészen szokatlan megoldást írtak le a Plos Biology lapban: Azt vizsgálták, mennyire hatékonyak a különböző antibiotikumok párosával alkalmazva. Az, hogy egyszerre két-három antibiotikummal kezeljünk egy fertőzést körülbelül azóta lebegő ötlet, amióta a második ilyen szert felfedezték, de ez a megoldás mégsem terjed el széles körben, egy-két nevezetes kivételtől eltekintve (malária, HIV, tuberkulózis) nem használják. Az akadálya az evolúció, a kórokozók folyamatosan evolválnak, ha már két hatóanyaggal szemben ellenállóak, hamar megjelennek a kettő ellen egyszerre ellenálló törzsek is.
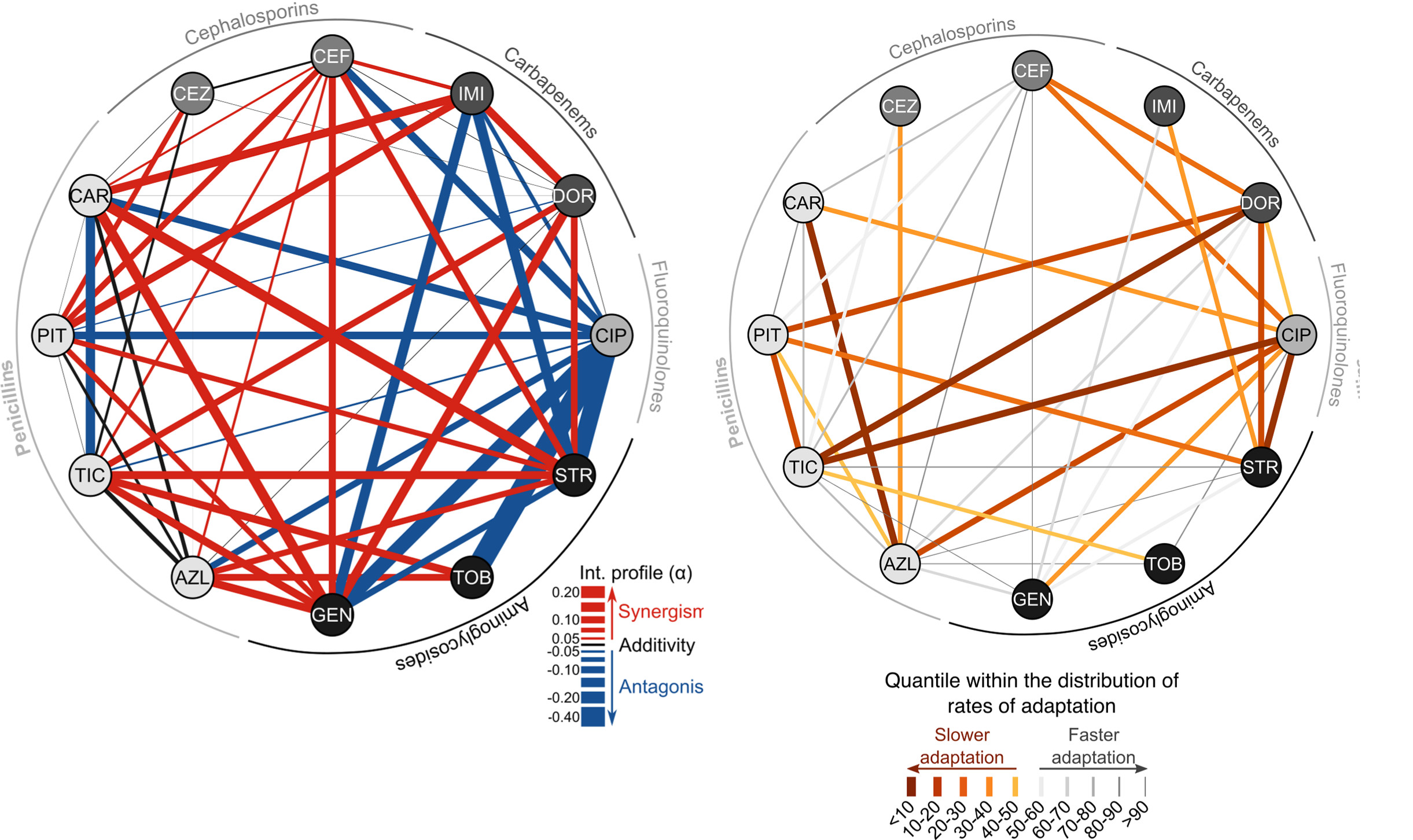
 A szerzők megfordították a jelenséget és felhasználták az evolúciót a minél hatékonyabb antibiotikumpárok feltérképezésére. A bal oldali ábra ezt mutatja, a külső körben az egyes antibiotikumok láthatóak, a szerzők kipróbálták mindegyiket mindegyik másikkal párosítva, a színes vonalak az egyes hatóanyagpárok Pseudomonas aeruginosa baktériumokra gyakorolt hatását mutatják. A piros vonalak azt mutatják, hogy a két antibiotikum egymás hatását erősíti, a kék vonalak jelentik, amikor a két hatóanyag egymás hatását gyengíti, a fekete vonalak jelzik, ha két hatóanyag semmilyen módon sem befolyásolja egymás működését. A vonalak vastagsága mutatja a hatás nagyságát, vagyis hogy melyik keverék mennyire gátolta a baktériumok növekedését, a legvastagabb piros vonalak (például a carbenicillin (CAR) és a streptomicin (STR) között) jelzik az egymás hatását leginkább erősítő párosításokat, míg a legvastagabb kék vonalak (például a ciprofloxacin (CIP) és a tobramycin (TOB)) jelzik az egymás hatását leginkább gyengítő hatóanyagokat. Eddig nem nagy felfedezés, hasonló munkákat mások is elvégeztek már.
A szerzők megfordították a jelenséget és felhasználták az evolúciót a minél hatékonyabb antibiotikumpárok feltérképezésére. A bal oldali ábra ezt mutatja, a külső körben az egyes antibiotikumok láthatóak, a szerzők kipróbálták mindegyiket mindegyik másikkal párosítva, a színes vonalak az egyes hatóanyagpárok Pseudomonas aeruginosa baktériumokra gyakorolt hatását mutatják. A piros vonalak azt mutatják, hogy a két antibiotikum egymás hatását erősíti, a kék vonalak jelentik, amikor a két hatóanyag egymás hatását gyengíti, a fekete vonalak jelzik, ha két hatóanyag semmilyen módon sem befolyásolja egymás működését. A vonalak vastagsága mutatja a hatás nagyságát, vagyis hogy melyik keverék mennyire gátolta a baktériumok növekedését, a legvastagabb piros vonalak (például a carbenicillin (CAR) és a streptomicin (STR) között) jelzik az egymás hatását leginkább erősítő párosításokat, míg a legvastagabb kék vonalak (például a ciprofloxacin (CIP) és a tobramycin (TOB)) jelzik az egymás hatását leginkább gyengítő hatóanyagokat. Eddig nem nagy felfedezés, hasonló munkákat mások is elvégeztek már.
A szerzők újítása, hogy ezek után egy evolúciós kísérletet is elvégeztek minden párosítással, vagyis százhúsz órán át hagyták a baktériumokat az adott gyógyszerpáros jelenlétében növekedni, tizenkét óránként friss táptalajra oltva őket. Ezek után vizsgálták meg, hogy melyik hatóanyagpáros mennyire hatékony a jelenlétéhez alkalmazkodott Pseudomona aeruginosa baktériumokon. Abból indultak ki, hogy minél nehezebben alkalmazkodik ez a szervezet egy hatóanyagpároshoz, annál nehezebben jelennek majd meg ellenálló törzsek a „vadonban” is, vagyis a gyakorlati gyógyászatban. Ennek az eredményét mutatja a jobb oldali ábra, az egyes vonalak azt mutatják, milyen gyorsan változott a baktériumok osztódási sebessége a kísérlet során az adott hatóanyagpáros jelenlétében. Azokat a hatóanyagpárosokat, amiknek a jelenlétében a jószágok először lassan osztódtak, de viszonylag hamar felgyorsult a szaporodásuk, szürkével jelölték, míg egyre sötétebb narancssárgával rajzolták fel azokat a párosokat, amelyekben kevéssé változott a baktériumok osztódási sebessége, azaz a kísérlet végén éppen olyan lassan osztódtak, mint az elején. Ezek a párosítások azok, amelyek kiállták a táptalajbeli evolúció próbáját, vagyis a Pseudomonas aeruginosa nehezen alkalmazkodott hozzájuk.
A kísérlet egészen meglepő eredményeket is hozott: Például a bal oldali ábrán látható módon a ticarcillin (TIC) a ciprofloxacinnal (CIP) vagy a piperacillinnel (PIP) együtt alkalmazva kismértékben gátolja egymás hatását, semmi különleges, ez alapján egyetlen ép eszű gyógyszergyártó sem próbálna meg engedélyeztetni egy ilyen gyógyszert. Viszont mindkét párosítás kifejezetten evolúcióállónak mutatkozott, várhatóan erre a kombinációra nagyon lassan alakulnak majd ki ellenálló baktériumtörzsek. Ugyanígy a carbenicillin (CAR) az azlocillinnel (AZL) semmilyen hatást sem fejt ki egymásra, a kölcsönhatásukat fekete vonal jelzi a bal oldalon, semmilyen okunk sem lenne együtt alkalmazni a kettőt, ám valamiért a Pseudomonas aeruginosa baktériumok nagyon nehezen alkalmazkodtak ehhez a pároshoz, időtálló gyógyszer válhat belőle. És ezen adatok alapján a legjobb választás a ticarcillin (TIC) és a doripenem (DOR) együttes alkalmazása lenne, ezek erősítik is egymás hatását és evolúcióállóak is.
Az itt leírt módszer egy különösen gyors (egy hét alatt elvégezhető egy ilyen kísérlet), költséghatékony módszert mutat be, amivel ötleteket kaphatnak a gyógyszerfejlesztők, hogyan használhatnak régebbi hatóanyagokat egészen újszerű kombinációkban, amikre maguktól akár nem is gondolnának.
Barbosa C, Beardmore R, Schulenburg H, Jansen G (2018) Antibiotic combination efficacy (ACE) networks for a Pseudomonas aeruginosa model. PLoS Biol 16(4): e2004356. https://doi.org/10.1371/journal.pbio.2004356

Csak 1 hét? Az tényleg nem sok, főleg ha ilyen meglepetésekkel szolgál. 🙂
Ha már antibaci koktél receptek szóba kerültek. A fenti antibacis párosításokat úgy képzeljem hogy mondjuk 5o% CAR + 5o% STR (és hogy most ez darab, térfogat, tömeg, telepszám … százalék azt nem is tudom). Csak azért kérdeztem, mert ha már koktél, lehet annak 2-nél több alkotórésze is, nyilván ekkor már sokkal több variációval kell számolni, de talán így több az ígéretes recept is.
@rdos: A koncentrációkat úgy állították be, hogy mindkét gyógyszer önmagában 75% -os gátlást adjon. Tehát könnyen lehet, hogy az egyikből egy gramot tettek a táptalajba, a másikból harmincat.
Nyilván meg lehetne próbálni hármasokat is, de ugye az eleve növeli a lehetséges kombinációk számát. Mindenesetre maga az elképzelés érdeke, főleg azért, hogy eddig miért nem alkalmazták? Hiszen például maláriaellenes szereknél teljesen természetes, hogy kétfélét kevernek.
@Sexcomb: Köszönöm a választ. Továbbá már az adagolás mikéntjét, vagy elvét is érteni vélem („erős paprikából kevesebb, mustárból több”). 🙂
A kettőnél több antibacis hatóanyagot azért dobtam be ötletként, mert ahogy pl. a gyomorban is több, vagy sok száz fajta baktérium él és végzi az emésztést, úgy akár elképzelhető olyan antibakteriális több összetevős „koktél”, ami még hatásosabban gátol. Azt értem hogy a variációk száma akár csak 12 hatóanyag esetén is kombinatorikailag számolható módon, de biztos hogy nagyságrendekkel növekszik, de hát valamit valamiért. A próba – szerencse vizsgálat már csak ilyen, de nem firtatom a kérdést tovább.
@rdos: Nyugodtan firtasd. Semmiképpen se fékezd a kíváncsiságodat!
Igazából világprobléma, hogy mit kezdjünk az antibiotikumoknak ellenálló baktériumokkal. Ez az egyik megoldás-javaslat, de korlátlan számú egyéb is elképzelhető.
Nagyon erdekes, koszonom a megosztast es kozertheto leirast! Sok nagyon meglepo adat van benne.
A cikk az orvosi felhasznalasra koncentral, de a szinergizmus es a ko-eovlucio mechanizmusa is nagy edeklodesre tarthat szamot, es tovabbi tanulmanyokat erne!
@fordulo_bogyo: No igen, ennek a sorozatnak az egyik hátránya, hogy egy cikkben csak egy, nagyon rövid gondolatot viszek végig, nem kalandozok el. Ettől lesz „Kezdőknek”.
@Sexcomb: Nem a te cikkedre gondoltam itt (es semmikeppen sem kritikakent irtam), hanem a szakmai publikaciora amit ismertettel. Gyorsan atfutottam, es ott sem mentek bele par odavetett mondaton tul, hogy mi lehet a kolcsonhatasok mechanizmusa.
Elsosorban az lepett meg, hogy a penicillinek poztivan egyuttmukodnek nemely mas antibiotikummal, hiszen a penicillinek csak a szaporodo bakteriumokat olik meg… azutan az is, hogy kep penicillinszarmazek gyengitheti egymas hatasat… szoval rengeteg erdekes apro reszlet van a cikkben, amiket erdemes lenne vizsgalni… egyfelol, mert nagyon izgalmas elmeleti kerdes, masfelol, mert akkor esetleg tudatosan tervezhetoek lehetnek majd a tobb komponensu koktelok ahol a szisztematikus minden kombinacio vizsgalata a lehetseges kombinaciok szama miatt nem elerheto.
Erdekes, az ember azt feltetelezne h ezt a vizsgalatot az elsok kozott vegeztek el mikor felmerult a rezisztens bakteriumok problemaja.
Bar ez a multirezisztencia velemenyem szerint csak a kovetkezmenye a tulnepesedesnek es a termeszet statisztikan alapulo valasza, hogy az egyensuly ismet meglegyen.
@Kiég3tt: Igazából meglepő, hogy nem. Az utolsó ötven-hatvan évben egyszerűen az új antibiotikumok kifejlesztésére összpontosított mindenki. Nyilván azért, mert volt még dögivel, viszonylag kis erőfeszítéssel találhattak új hatóanyagokat. Mostanra jutott odáig a helyzet, hogy nagyon nehezen találnak már új, eddig ismeretlen hatóanaygokat. Ráadásul a gyógyszerek könyörtelen logikája szerint egy új antibiotikumot rögtön utolsó vonalbeli szernek minősítenek, mindenféle moratóriummal akadályozzák a használatát. Ellenben a régi szerek újrakeverése várhatóan nem jár ezzel a hátránnyal.
Igazából az evolúció így működik: Bármilyen szelekciós nyomást adsz egy rendszerre, azt követve evolvál majd. Ha gyomirtóval irtasz növényeket, megjelennek a gyomirtóknak ellenálló gyomok. Ha antibiotikummal irtasz baktériumokat, megjelennek az antibiotikumoknak ellenálló bacik.
Kössz ez nagyon tetszett. Hasonló cikk a témában, amiben szintén erre a következtetésre jutnak, hogy a fenyegető antibiotikum rezisztencia kivédésének hatékony módja lenne a hatóanyagok kombinációja. [Drug combinations: a strategy to extend the life of antibiotics in the 21st century; Nature Reviews Microbiology 17, 141–155 (2019)] Kifejtik, hogy a rezisztencia kialakulását meg lehetne nehezíteni, ha az eddigi gyakorlat, egy szerrel egy ponton beavatkozni helyett, az egy szerrel több ponton beavatkozni elvet követnénk. Mivel ilyen szerek kifejlesztése meglehetősen nehéz feladat, ezért megoldás lenne a több ponton ható (különböző hatásmechanizmussal rendelkező) gyógyszerkombinációk alkalmazása. Ez például megdöbbentett: „…previous studies have uncovered important and often non-obvious antibiotic interactions. These include the observations that antagonistic drug pairs can suppress resistance, that synergistic combinations can counterintuitively drive more rapid evolution of resistance than individual antibiotics, that alternating drug treatments can be more efficacious than co-treatment and that higher-order combinations can lead to dose orthogonality that is difficult to model and can often result in unexpected interactions.”