 Amióta felpörgött a COVID-19 járvány, néha felröppen egy-egy cikk arról, hogy megtalálták a vírus ellenszerét, valamilyen ellenanyagot. Mivel az ellenanyagot angolul ″antibody″ -nak hívják, néha a sajtóban antitestként is emlegetik. De akkor miért nincs belőle még gyógyszer? Azért érdekes kérdés, mert ezekkel párhuzamosan a leghajmeresztőbb összeesküvés-elméletek keltek szárnyra, igazán tekintélyes filozófusok ekézték a gyógyszergyárakat az ellenanyagok miatt. De akkor mi a helyzet ezekkel az ellenanyagokkal? Miért nem készült belőlük gyógyszer?
Amióta felpörgött a COVID-19 járvány, néha felröppen egy-egy cikk arról, hogy megtalálták a vírus ellenszerét, valamilyen ellenanyagot. Mivel az ellenanyagot angolul ″antibody″ -nak hívják, néha a sajtóban antitestként is emlegetik. De akkor miért nincs belőle még gyógyszer? Azért érdekes kérdés, mert ezekkel párhuzamosan a leghajmeresztőbb összeesküvés-elméletek keltek szárnyra, igazán tekintélyes filozófusok ekézték a gyógyszergyárakat az ellenanyagok miatt. De akkor mi a helyzet ezekkel az ellenanyagokkal? Miért nem készült belőlük gyógyszer?
Az ellenanyagok a gerinces immunrendszer egyik alapvető elemei, a szervezetünk termeli őket. Egy ellenanyag egy fehérjemolekula, ami úgy működik, hogy vizes oldatban felismer egy bizonyos molekuláris mintázatot, általában egy másik fehérje egy rövidebb szakaszát és erősen hozzáköt. A vírusfertőzések esetén ez életmentő, hiszen ha például a vérünkben olyan ellenanyagok keringenek, amik felismerik a vírus valamilyen felületi fehérjéjét, akkor a szervezetünkbe jutó vírusrészecskékre azonnal rátapadnak, körbeveszik, így megakadályozzák, hogy azok bejussanak a sejtjeinkbe, ezzel véget is vetnek a fertőzésnek. Ezért segíthet a COVID-19 fertőzésen ha a betegnek beadják egy, a fertőzésen éppen átesett ember vérét, mivel a fertőzésből nemrég felgyógyult ember vérében még nagyon sok ellenanyag kering, amik felismerik a vírusrészecskéket és akadályozzák a működését. Ezek a beteg szervezetébe kerülve ugyanúgy működnek majd, éppen úgy gátolják a vírus szaporodását, ezzel lassítva a fertőzést.
Itt ugye egy figyelmes olvasóban rögtön fölmerül a kérdés, hogy ha a szervezetünk termel ellenanyagokat, amik működésképtelenné teszik a COVID-19 részecskéket, akkor miért léteznek egyáltalán fertőzések? A válasz egyszerű: a szervezetünk nem születésünktől kezdve termel ellenanyagokat például a COVID-19 vírus ellen, csak miután már találkoztunk vele. Az ellenanyagokat a vérünkben keringő B-sejtek termelik, mivel az ellenanyagok fehérjetermészetűek, kézenfekvő módon egy, a B-sejt genomjában található génről íródik át ez a fehérje. Egyetlen B-sejt egyetlen ellenanyagot termel, ami egyetlen molekuláris mintázatot ismer fel. Amennyiben osztódik, a leánysejtjei is ugyanazt az ellenanyagot termelik majd. Viszont a vérünkben szédítő mennyiségű ellenanyag kering folyamatosan, minden kórokozó, amivel valaha találkoztunk tucatnyi különböző, ellene hatásos ellenanyag termelését indította be életünk során, viszont az emberi genom pár tízezer gént tartalmaz, egyáltalán nem férne bele az a milliárdnyi különböző ellenanyagot kódoló gén. Ennek megfelelően minden egyes ellenanyagot egyetlen B-sejt (és a leánysejtjei) termelnek. A B-sejtek érésük során egy, a gerincesek között egyébként ismeretlen folyamaton esnek át, a genomban kódolt génszakaszokból véletlenszerűen összeszerelnek egy gént, ami egy egyedi ellenanyagot kódol. Mivel a frissen létrejött gén véletlenszerű folyamatok eredménye, nyilván a legtöbb így keletkező ellenanyag semmit sem ismer föl, vagy olyan molekuláris mintázatot, ami éppen nincs jelen a szervezetben, esetleg egy saját fehérjét. Éppen ezért a naponta érő milliónyi B-sejt mindegyike átesik egy kiválasztási folyamaton, ahol elpusztulnak azok, amik semmit sem ismernek fel és azok is, amelyek saját molekuláris mintázatot felismerő ellenanyagot termelnek. Csak az a kevés B-sejt marad meg, amelyek valami olyan mintázatot felismerő ellenanyagot termelnek, ami külső forrásból származik, vélhetőleg egy éppen támadó kórokozó részei. Ezek a sejtek viszont osztódni kezdenek és a leánysejtjeik évtizedeken át megmaradnak, bármikor újra megjelenik a szervezeteben a kórokozó, amivel egyszer már találkoztunk, azonnal ellenanyagokat termelnek ellene. Ez a magyarázata, hogy miért kaphatunk el egy csomó betegséget életünkben csak egyszer: Amikor először találkozunk egy kórokozóval, még nem termel a szervezetünk az adott mikróbát felismerő ellenanyagokat, átlagosan két hétbe telik, mire a véletlenszerűen előállított gének közül akad néhány, ami olyan ellenanyagot kódol, ami pont felismeri az éppen támadó kórokozót és annyit osztódik, hogy már jelentős mennyiségű ellenanyagot termelnek meg a leánysejtjei.
 Ebből következik, hogy az ellenanyagok tényleg ″mindenre jó″ gyógyszerként működnek, bármilyen kórokozó ellen néhány hét alatt előállíthatóak azt semlegesítő ellenanyagok, akármilyen gerinces állatban. Erről szólnak az ilyen cikkek, hogy találtak egy koronavírus ellen is hatásos ellenanyagot. De ha minden ilyen szép és jó, akkor miért nincs még belőle gyógyszer, miért potyogtathatnak még mindenféle összeesküvés-elméletet arról, hogy visszatartják a gyógyszert? A válasz az ellenanyag-kezelések története adja meg. A kézenfekvő megoldás, hogy a koronavírus fertőzésből frissen felgyógyult emberek vérét adják be betegeknek láthatóan döcögősen halad, nyilván kell hozzá megfelelő véradó és ilyenkor a fertőzésveszéllyel is számolniuk kell, így ezek a kezelések sohasem válnak majd tömegessé. De az immunrendszer itt vázolt működése elég régóta ismert, ennek megfelelően elég régóta próbálkoznak már a gyógyszerként felhasználásukkal is. Az első kereskedelmi forgalomban is kapható ilyen gyógyszer a diftéria elleni ellenanyagból készült, akkoriban úgy hívták, antitoxin. Az eljárást Emil von Behring és Kitasato Shibasaburo dolgozták ki 1890 -ben, ám 1894 -ben már forgalomba is került az általuk gyártott ellenanyag. Az elkészítése során lovakat oltottak be a diftériát okozó baktérium egyik fehérjéjével, amik így néhány hét alatt ellenanyagokat kezdtek termelni az idegen fehérje ellen. Ekkor vért vettek tőlük, amiből leválasztották a sejtes elemeket, a maradék vérsavót tisztították, ezt forgalmazták gyógyszerként, amit injekcióban adtak be diftériás gyerekeknek. A ló ellenanyagok ugyanúgy működtek az emberi szervezetben is, működésképtelenné tették a baktérium által termelt mérget, így jelentősen csökkentették a betegség súlyosságát, elég jó hatásfokkal mentették meg a gyerekek életét. Ez akkoriban jelentős tudományos áttörésnek számított, sorra készültek a hasonló elven működő gyógyszerek, például tetanusz antitoxint 1910 -től már széles körben használták. (Mint a korabeli karikatúrából kikövetkeztethető, a kortársak nem mindannyian lelkesedtek a forradalmi találmányért.) A technológia nem tűnt el teljesen, például a mai napig forgalmaznak ellenanyagokat kígyómarás kezelésére, amik ugyanezen az elven működnek, kígyóméreggel beoltott lovakban termelődő ellenanyagokat oltanak be a megmart emberekbe. Azonban ennek a kezelésnek a mellékhatásai sem elhanyagolhatóak. Mivel mégiscsak egy csomó ló eredetű fehérjét oltatnak a szervezetbe, ezeket az emberi immunrendszer idegen fehérjeként ismeri fel, így ezek ellen is immunválasz indult. Az első alkalommal ez általában nem számít, kiürülnek a ló fehérjék, még mielőtt súlyos tüneteket okoznának, a problémák akkor jelentkeznek, ha többször is ló vérsavóból készült gyógyszert adtak be ugyanannak az embernek. Tehát nem nagyon lehetett teszem azt egy gyereket minden gyermekbetegség ellen ellenanyagokkal kezelni, mert a második-harmadik kezelésre már a ló fehérjék elleni immunválasz is könnyedén megölheti a beteget. Ilyen esetek még manapság is történnek, például 2001 -ben halt meg Magyarországon egy férfi, aki kígyómarás után beadta magának a kígyóméreg elleni savót, de mivel már korábban is többször kezelték ló eredetű szerekkel, így a ló szérum elleni immunválasz ölte meg. Mivel manapság ilyen mellékhatásokkal rendelkező gyógyszerek gyakorlatilag sohasem kapnak engedélyt az egészségügyi hatóságoktól, így nem várható, hogy ezzel a kétségtelenül gyorsan rendszerbe állítható módszerrel termeljen bárki is koronavírus elleni ellenanyagokat, bár kétségkívül rendelkezésre áll a technológia. Egyéb, talán nem kézenfekvő gátjai is lehetnek ennek a termelésnek, például az ezernyolcszázas évek végén rengeteg lovat használtak a nyugati világban is, az első ilyen ellenanyaggyárakban kiszolgált igáslovakkal kezdték meg a termelést, nyilvánvalóan ezekhez jóval olcsóbban jutottak hozzá, mint amibe manapság kerülne egy ilyen ménes összeállítása.
Ebből következik, hogy az ellenanyagok tényleg ″mindenre jó″ gyógyszerként működnek, bármilyen kórokozó ellen néhány hét alatt előállíthatóak azt semlegesítő ellenanyagok, akármilyen gerinces állatban. Erről szólnak az ilyen cikkek, hogy találtak egy koronavírus ellen is hatásos ellenanyagot. De ha minden ilyen szép és jó, akkor miért nincs még belőle gyógyszer, miért potyogtathatnak még mindenféle összeesküvés-elméletet arról, hogy visszatartják a gyógyszert? A válasz az ellenanyag-kezelések története adja meg. A kézenfekvő megoldás, hogy a koronavírus fertőzésből frissen felgyógyult emberek vérét adják be betegeknek láthatóan döcögősen halad, nyilván kell hozzá megfelelő véradó és ilyenkor a fertőzésveszéllyel is számolniuk kell, így ezek a kezelések sohasem válnak majd tömegessé. De az immunrendszer itt vázolt működése elég régóta ismert, ennek megfelelően elég régóta próbálkoznak már a gyógyszerként felhasználásukkal is. Az első kereskedelmi forgalomban is kapható ilyen gyógyszer a diftéria elleni ellenanyagból készült, akkoriban úgy hívták, antitoxin. Az eljárást Emil von Behring és Kitasato Shibasaburo dolgozták ki 1890 -ben, ám 1894 -ben már forgalomba is került az általuk gyártott ellenanyag. Az elkészítése során lovakat oltottak be a diftériát okozó baktérium egyik fehérjéjével, amik így néhány hét alatt ellenanyagokat kezdtek termelni az idegen fehérje ellen. Ekkor vért vettek tőlük, amiből leválasztották a sejtes elemeket, a maradék vérsavót tisztították, ezt forgalmazták gyógyszerként, amit injekcióban adtak be diftériás gyerekeknek. A ló ellenanyagok ugyanúgy működtek az emberi szervezetben is, működésképtelenné tették a baktérium által termelt mérget, így jelentősen csökkentették a betegség súlyosságát, elég jó hatásfokkal mentették meg a gyerekek életét. Ez akkoriban jelentős tudományos áttörésnek számított, sorra készültek a hasonló elven működő gyógyszerek, például tetanusz antitoxint 1910 -től már széles körben használták. (Mint a korabeli karikatúrából kikövetkeztethető, a kortársak nem mindannyian lelkesedtek a forradalmi találmányért.) A technológia nem tűnt el teljesen, például a mai napig forgalmaznak ellenanyagokat kígyómarás kezelésére, amik ugyanezen az elven működnek, kígyóméreggel beoltott lovakban termelődő ellenanyagokat oltanak be a megmart emberekbe. Azonban ennek a kezelésnek a mellékhatásai sem elhanyagolhatóak. Mivel mégiscsak egy csomó ló eredetű fehérjét oltatnak a szervezetbe, ezeket az emberi immunrendszer idegen fehérjeként ismeri fel, így ezek ellen is immunválasz indult. Az első alkalommal ez általában nem számít, kiürülnek a ló fehérjék, még mielőtt súlyos tüneteket okoznának, a problémák akkor jelentkeznek, ha többször is ló vérsavóból készült gyógyszert adtak be ugyanannak az embernek. Tehát nem nagyon lehetett teszem azt egy gyereket minden gyermekbetegség ellen ellenanyagokkal kezelni, mert a második-harmadik kezelésre már a ló fehérjék elleni immunválasz is könnyedén megölheti a beteget. Ilyen esetek még manapság is történnek, például 2001 -ben halt meg Magyarországon egy férfi, aki kígyómarás után beadta magának a kígyóméreg elleni savót, de mivel már korábban is többször kezelték ló eredetű szerekkel, így a ló szérum elleni immunválasz ölte meg. Mivel manapság ilyen mellékhatásokkal rendelkező gyógyszerek gyakorlatilag sohasem kapnak engedélyt az egészségügyi hatóságoktól, így nem várható, hogy ezzel a kétségtelenül gyorsan rendszerbe állítható módszerrel termeljen bárki is koronavírus elleni ellenanyagokat, bár kétségkívül rendelkezésre áll a technológia. Egyéb, talán nem kézenfekvő gátjai is lehetnek ennek a termelésnek, például az ezernyolcszázas évek végén rengeteg lovat használtak a nyugati világban is, az első ilyen ellenanyaggyárakban kiszolgált igáslovakkal kezdték meg a termelést, nyilvánvalóan ezekhez jóval olcsóbban jutottak hozzá, mint amibe manapság kerülne egy ilyen ménes összeállítása.
A következő szűk száz évben természetesen rengeteget finomítottak az ellenanyagok előállításán, ezeket be lehetne vetni egy ilyen termék elkészítéséhez. A kézenfekvő megoldás, nyilván az, hogy a ló savóban keringő rengeteg fehérje közül valahogyan kiválasztjuk az ellenanyagokat. Ezzel máris nagy lépést tettünk előre, az ilyen készítmény eleve sokkal kevésbé vált ki immunválaszt az emberi szervezetből, mivel kevesebb különböző fehérjét tartalmaz. Az egyik furmányos trükk, amit bevethetne egy reménybeli gyártó egy baktériumból származik. A neve protein G, így nem sokat mond, ez egy kórokozó baktérium által termelt fehérje, ami egészen szokatlan feladatot lát el a baktériumban: megköti az ellenanyag fehérjéket, így a baktérium felületéhez köti őket, de nem az egyébként a kötésért felelős szakaszán, hanem éppen a fehérje ellentétes végén. Így a baktérium mintegy elbújik az immunrendszer elől, ellenanyagokkal burkolja be magát, ám megakadályozza, hogy azok beindítsák az immunválaszt, mivel éppen az ellenanyag fehérjék éppen ehhez szükséges végét köti meg. Ez a fehérje ugyanezt a működést a baktériumon kívül is elvégzi, ha valamilyen szilárd hordozóhoz kötjük és azon átfolyatjuk a szérumot, a protein G megköti az ellenanyagokat, de az összes többi fehérje akadálytalanul átfolyik az oszlopon. Később a mosófolyadék változtatásával a protein G szerkezete megváltoztatható, ekkor elengedi az ellenanyagot, ami így lemosható az oszlopról. Ezzel az apró trükkel elválaszthatóak az ellenanyagok a savó többi fehérjéjétől, máris megszabadultunk egy csomó olyan alkotóelemétől, ami immunválaszt váltana ki. Ekkor már csak az ellenanyagok maradnak az oldatban, de ugye ez számtalan különböző molekuláris mintázatot felismerő ellenanyagot jelent. Még bevethetünk egy elválasztási lépést, és hasonlóképpen egy oszlophoz kötve koronavírus részecskéket, kiválaszthatjuk az ellenanyagok közül azokat, amik a vírusrészecskéket ismerik fel. Ezzel ugyan a termékünk egyre tisztábbá válik, egyre kevesebb fölösleges fehérjét tartalmaz, de a vége mégis egy ló eredetű ellenanyag marad, ami valamilyen immunválaszt válthat ki. Ráadásul mivel minden adag egy-egy újabb állat szervezetében lezajlott véletlenszerű immunválasz eredménye, nagyon nehéz állandó minőséget termelni belőlük, amit a mai gyógyszeripar elvárna. És minden egyes elválasztási lépés emeli a költségeket. Nem valószínű, hogy ilyen terméket bárki is piacra dobna, bár a technológia már száz éve létezik, semmi elméleti akadálya sincs, hogy koronavírus fertőzést lósavóval gyógyítsunk.
Az ellenanyagok gyógyszerként alkalmazásában a következő áttörést Jerrold Schwaber és Edward Cohen érte el 1973 -ban. Ők egy olyan módszert találtak ki, amellyel mintegy rendelésre készíthetőek ellenanyagok, az emlős immunrendszer működésének kihasználásával. Egereket oltanak be azzal a fehérjével, amit felismerő ellenanyagot szeretnének létrehozni, majd miután kialakult az immunválasz, az egér lépéből nyert B-sejteket egy egér daganat sejtvonal sejtjeivel olvasztják össze, így olyan sejteket nyernek, amik korlátlanul képesek osztódni és egy sejt utódai mind hajszálra ugyanazt az ellenanyagot termelik majd, bármennyit is osztódnak. Ezek a sejtvonalak tápoldatban fönntarthatóak és velük egyetlen egy ellenanyag fehérje termeltethető akár kilószámra is, minden egyes fehérjemolekula ugyanúgy működik majd, ugyanazt a molekuláris mintázatot ismeri fel. Ezeket nevezik monoklonális ellenanyagoknak. Ennek a megoldásnak az előnye, hogy itt már csak egyetlen egy ellenanyagot termelnek a sejtek, az élő állatokból nyert ellenanyagok változatosságát rögtön nullára csökkenti, így sokkal kevésbé indít immunválasz egy ilyen készítmény ellen az emberi szervezet, hiszen sokkal kevesebb idegen fehérjét juttatunk be egy ilyen injekcióval. Ezekből már gyógyszerek is kaphatók, sőt a gyógyszeripar felívelő területének számítanak, mivel ezzel a megoldással garantálható az állandó minőség, mivel gyakorlatilag azonos sejtek termelnek gyakorlatilag azonos ellenanyagot, minden adag ugyanúgy működik. Ilyen gyógyszerek kaphatóak ma is, szemérmetlenül magas áron, a blinatumomab például adagonként négyezer dollárba kerül. A módszer legnagyobb hátránya, hogy csak egérben működik, az ehhez szükséges daganatsejtvonalat csak egérben sikerült megtalálni. Ez egyelőre a nem-irányított módszerek végső határa.
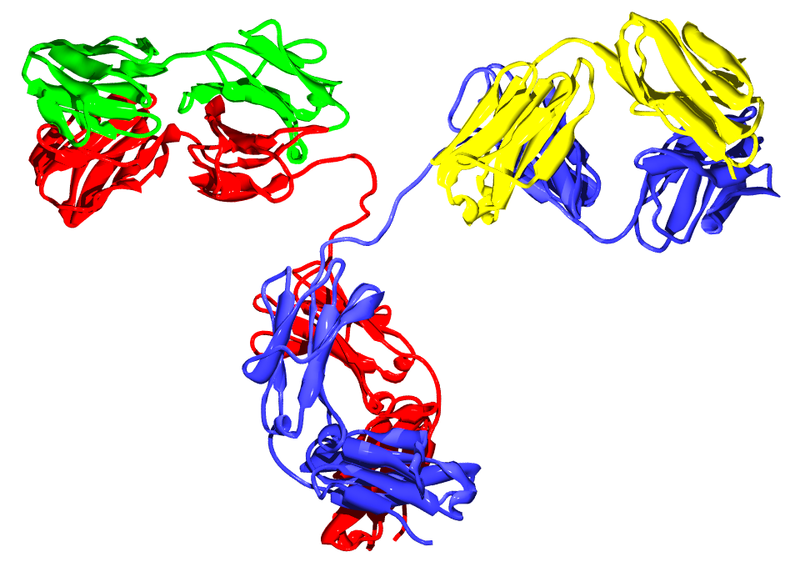
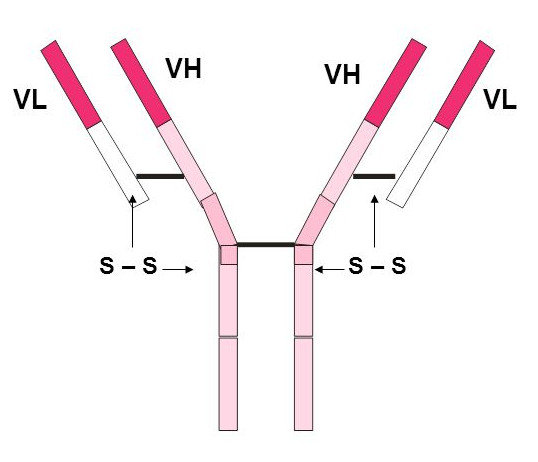
Viszont a rekombináns DNS technológia (=génmódosítás) megjelenésével az ellenanyagok gyógyszerként felhasználása is óriási lendületet kapott. Itt érdemes megállni és kicsit alaposabban megnézni, mik is ezek az ellenanyagok, amikről eddig csak annyit árultam el, hogy fehérjék? A képen egy ellenanyag molekula szerkezete látható, egy jellegzetes, Y alakú működési egység négy fehérjeláncból áll, két egyforma nehéz láncból és két egyforma könnyű láncból. A nehéz és a könnyű láncot is egy-egy gén kódolja a B-sejt genomjában, mindkettő hasonló véletlenszerű génátrendeződés eredménye. Viszont ettől a különböző B-sejtek által termelt nehéz- és könnyű láncoknak csak egy rövidebb szakasza változékony, ez látszik az ábrán rózsaszínnel, ez felelős a molekuláris mintázat kötéséért, mindkét lánc jelentős része azonos a különböző ellenanyag molekulákban. Az ellenanyag működéséhez mindkét fehérjelánc szükséges, a két lánc változékony szakaszai együttesen alakítják ki a molekuláris mintázatot felismerő antigénkötő zsebet.
A kézenfekvő megoldás, ami rögtön egyszerűsíti az ellenanyagok gyógyszerként felhasználását, ha az egér sejtvonalból, ami eredetileg termelte, a két fehérjeláncot kódoló két gént áthelyezik egy emberi sejtvonalba. Így máris olyan sejtek termelik az ellenanyagot, amik emberi eredetűek, rögtön kevesebb állati eredetű termék szennyezi a mintát, könnyebb, vagyis olcsóbb előállítani a terméket. De ugye ez attól még mindig egy egér ellenanyag marad. Viszont megoldható, hogy nem a teljes fehérjeláncot kódoló génszakaszt ültetik át az emberi sejtvonalba, hanem az egér eredetű géneknek csak a molekuláris mintázatot felismerő szakaszait, a nem változékony szakaszokat emberi ellenanyagok hasonló szakaszaival helyettesítik. Az eredmény egy ellenanyag molekula, ami ugyanazt molekuláris mintázatot ismeri fel, mint az eredeti egér ellenanyag, csak éppen két egészen rövid szakasza egér eredetű, egy ilyen ellenanyag emberbe oltásakor máris sokkal kevesebb idegen fehérjét juttatunk be, hiszen még a monoklonális ellenanyagunk nagy része is emberi eredetű, máris jelentősen csökkent az esélye, hogy az emberi szervezet immunválaszt indítana ellene. Ezeket nevezik humanizált ellenanyagoknak.
A monoklonális ellenanyagok létrehozása azért ilyen körülményes, mert a B-sejtek, mint a testi sejtek általában nem osztódhatnak végtelen számút, néhány megkettőződés után elöregednek és nem szaporodnak tovább. Ezért szükséges a halhatatlan egér sejtvonallal összeolvasztani őket, a daganatsejtek teszik lehetővé, hogy korlátlanul osztódhasson a létrejövő sejtvonal. Ellenben az előző bekezdés nyomán már elgondolkodhatott az olvasó, hogy tulajdonképpen minek is ez a bonyolult megoldás? Valóban, megoldható például, hogy magukat a B-sejteket egyesével tenyésztik egy-egy apró műanyagedényben, ekkor a sejtek ugyan csak néhányszor osztódnak, de annyi sejt éppen elég ahhoz, hogy az általuk termelt ellenanyagot kódoló két gént azonosítsák és egy már meglévő daganatsejtvonalba ültetve azzal ellenanyagot termelhessenek. Így bármilyen gerincesből készíthetőek ellenanyagok, például emberekből is, a világon semmi akadálya sincs, hogy egy COVID-19 fertőzésen átesett betegtől néhány cső vért levéve megkeressék és korlátlan mennyiségben megtermeltessék az ő szervezetében kialakult, a fertőzést legyőző ellenanyagokat. Ebben az esetben már semmilyen állati eredetű fehérjét sem tartalmaz a rendszer, egészen minimális eséllyel alakulhat ki a szervezetben immunválasz a beoltott ellenanyag ellen.
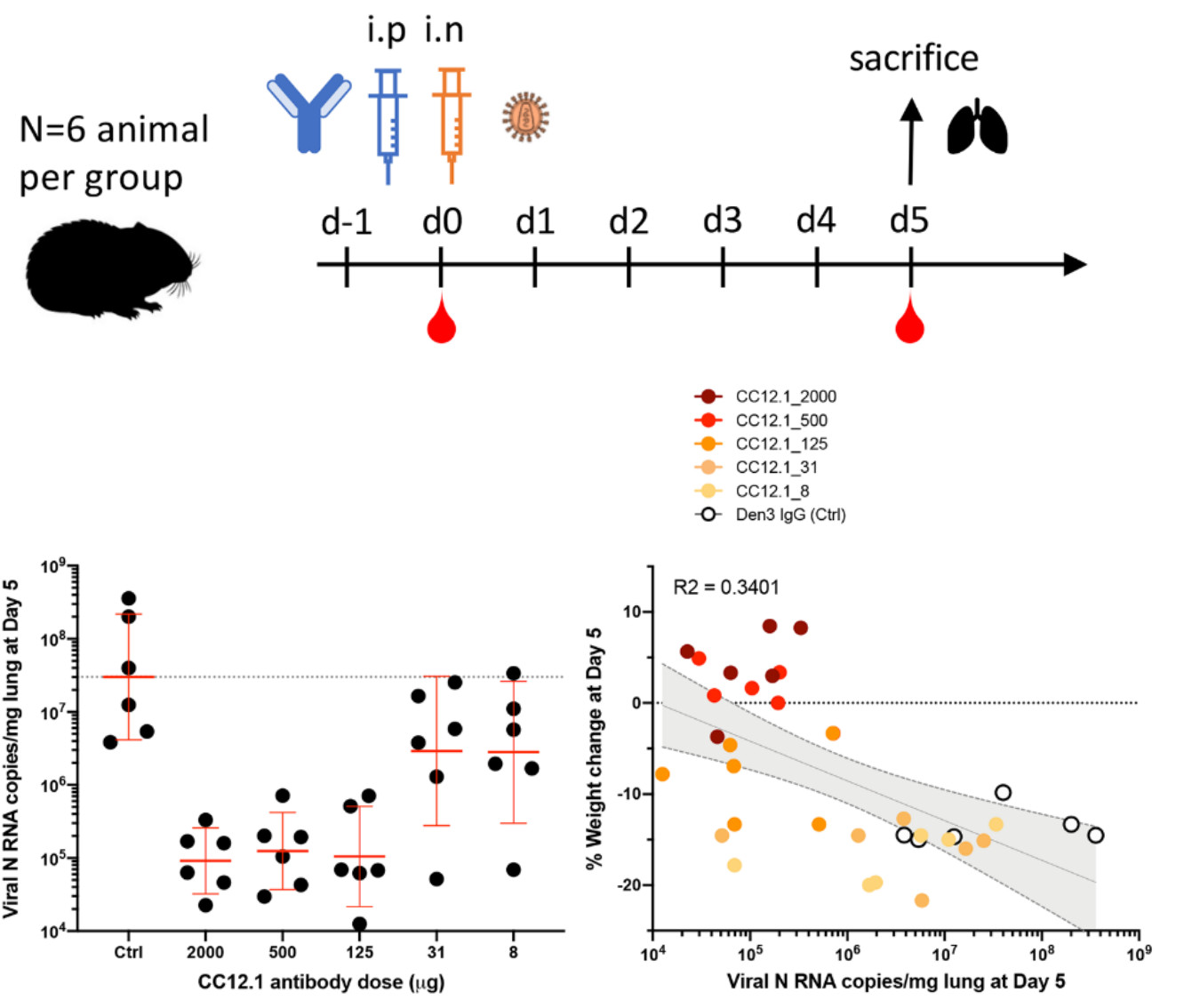
Például egy ilyen megközelítést közölt le Rogers és munkatársai három napja a Science című folyóiratban. Ők eleve Sars-CoV-2 fertőzésen átesett embereket kerestek, az ő vérmintáikból ellenanyagot termelő B-sejteket gyűjtöttek, majd a betegektől vérmintát vettek. Mivel ők már egy lépéssel korszerűbb módszert választottak, még az előző bekezdésben említett sejttenyésztéssel sem foglalkoztak, egyszerűen egyesével leválogatták a betegek B-sejtjeit és minden egyes sejt két ellenanyag nehéz- illetve könnyű láncát kódoló génjét párosával áthelyezték egy sejtvonalba, majd rögtön meg is termeltették az ellenanyagokat. Összesen tizenhét betegből előállított ezernyolcszáz ellenanyagot vizsgálták végig, hogy melyikük teszi hatékonyabban működésképtelenné s Sars-CoV-2 vírusrészecskéket. A legjobban működő ellenanyagot kipróbálták egy szír aranyhörcsög fertőzési rendszerben is, a hörcsögök a termelt ellenanyagból kaptak különböző mennyiséget, az első csoport semmit, a második csoport 2 milligrammot, a többiek mindig négyszer kevesebbet (500 μg, 125 μg, 31 μg, 8 μg). Ezek után fertőzték a hörcsögöket Sars-CoV-2 vírussal, majd öt nap múlva megmérték, hány példányt találni a vírus genomból az állatok tüdejében. Nem meglepő módon a legtöbb ellenanyaggal beoltott hörcsögökben körülbelül ezredannyi vírust mutattak ki, mint a kezeletlenekben, de még ennek a mennyiségnek a tizenhatoda (125 μg) is ugyanennyire védett a fertőzéstől, csak a két milligrammos adag egyhatvannegyedével beoltott hörcsögökben találtak nagyobb mennyiségű vírusrészecskét. Ezt mutatja a második ábra bal oldala. A jobb oldalon az állatok fogyása látható, ami a betegségük súlyosságát mutatja. Várhatóan a kezelést nem kapott állatok fogytak le a legjobban, míg a legtöbb ellenanyagot kapó csoport tagjai még híztak is egy kicsit a kísérlet alatt.
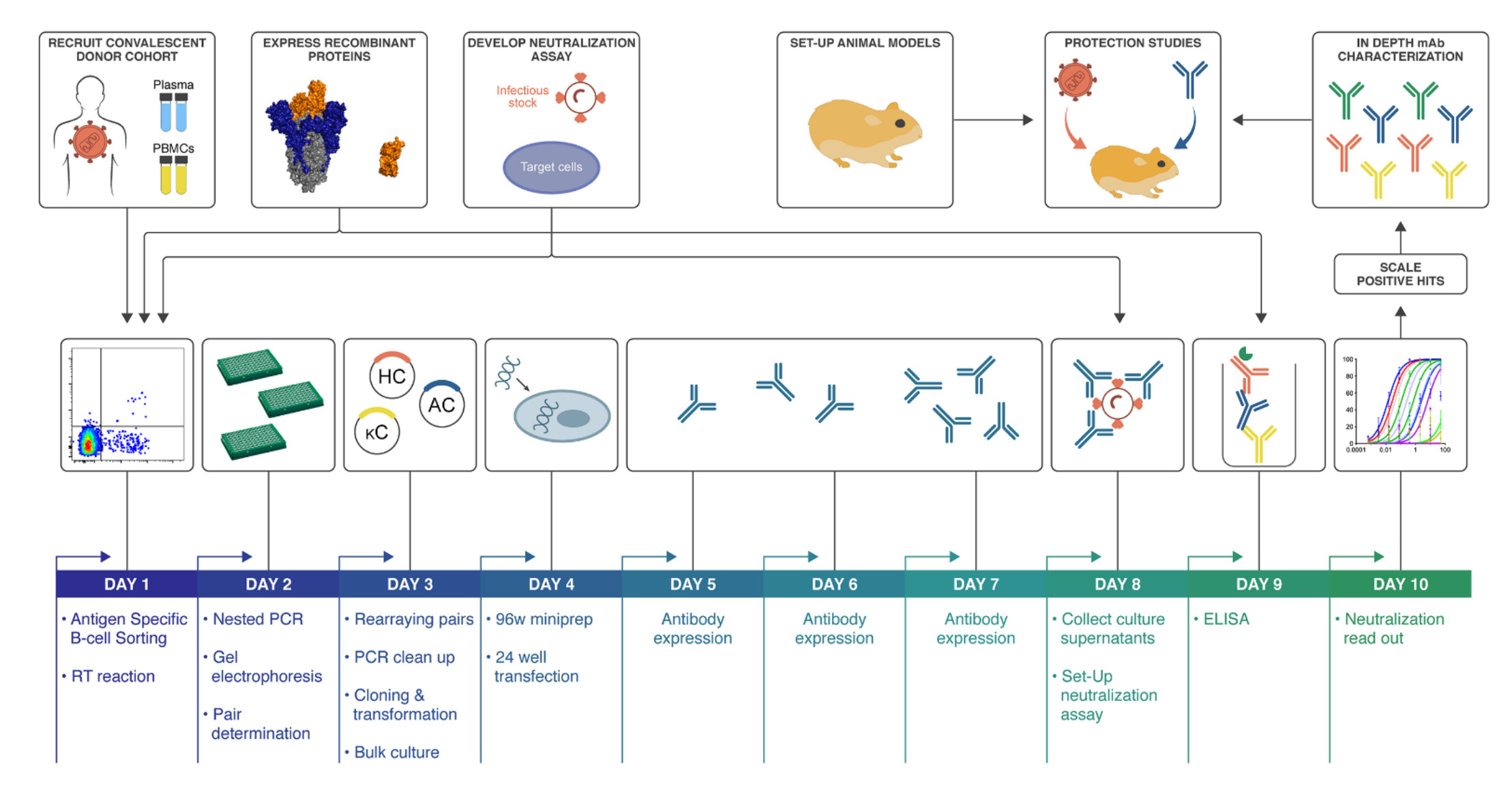
Ami igazán döbbenetes és a rekombináns DNS technológia behozhatatlan előnyét mutatja: Onnantól, hogy megszúrták a gyógyult COVID-19 -es betegeket kerek tíz napba tellett, mire odáig eljutottak, hogy az első ellenanyagok működését is vizsgálhatták vírusrészecskéken.
A kérdés megmarad, hogy ha ilyen veszett egyszerű és gyors bármilyen vírus ellen hatásos ellenanyagokat fejleszteni, akkor miért ülünk mégis hónapok óta karanténban? A válasz kézenfekvő, ha a fenti kísérlet egy jól működő dózisát vesszük alapul, a Rogersék által talált ellenanyagból testsúlykilogrammonként négy milligramm fehérje kellene, egy száz kilós embernek majdnem fél gramm. Jelenleg a teljes monoklonális ellenanyag gyártó kapacitás a Földön évi pár tucat tonna, vagyis ha minden ilyen üzemet most azonnal átállítanánk ennek az egy ellenanyagnak a termelésére, akkor egy év alatt sikerülne néhány tucat millió adagot gyártani belőle (20-60 milliószor fél grammot). És mindez olyan százhatvan milliárd dollárba kerülne, ami több, mint Magyarország teljes GDP -je. De hogyan lehetne feltornászni a monoklonális ellenanyagtermelést, ha már ilyen hasznos? Hogyan lehetne ezeket a vérfagyasztóan magas árakat letörni? Na, erről legközelebb írok majd!
Szeretnék a „valódi” sajtóba írni szabadúszóként, de sajnos kívülről bekerülni szinte lehetetlen. Úgyhogy ha újságíró, szerkesztő, laptulajdonos, stb. vagy és szívesen látnád a tudományos ismeretterjesztő cikkeimet a lapodban, bátran keress meg! janoszsambokibio@gmail.com
Rogers, T. F., Zhao, F., Huang, D., Beutler, N., Burns, A., He, W. T., … & Yang, L. (2020) Rapid isolation of potent SARS-CoV-2 neutralizing antibodies and protection in a small animal model. Science doi: 10.1126/science.abc7520

Tegnap olvastam, hogy a méhészek a méh-szúrások miatt nem voltak fertőzöttek sem Kínában sem Németországban.
Visszajelzés: Hogyan duplázhatnánk meg a magyar GDP -t? – CriticalBiomass