 Ha igazán elegáns struktúrát keresünk egy gerinces élőlényben, a retina minden valószínűség szerint dobogós helyezést fog elérni.
Ha igazán elegáns struktúrát keresünk egy gerinces élőlényben, a retina minden valószínűség szerint dobogós helyezést fog elérni.
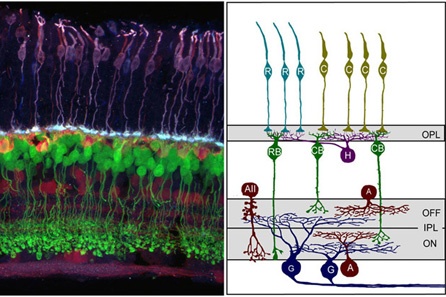
A fényérzékeny fotoreceptorokból és "kapcsolt részeikből" kialakuló hálózat egyszerű szövettani metszetén (emlősök esetében) tíz jól elkülönülő réteget fedezhetünk fel, aszerint, hogy adott rétegben az egyes sejtek magjai, vagy pedig nyúlványai helyezkednek el. Jobban megpiszkálva látható az is, hogy a tíz réteg igazából laza definícióban öt sejttípust rejt: a fotoreceptorokat (amelyek persze lehetnek csapok (C) vagy pálcikák(R)), az ingerületet a retinából az agyba szállító ganglionsejteket (G), az előbbi kettőt összekötő ún. bipoláris sejteket (ezeket részletesebb leírásokban két csoportra osztják aszerint, hogy csapokhoz vagy pálcikákhoz kapcsolódnak (CB ill RB)), illetve az említett három sejttípus kapcsolatát moduláló horizontális- (H), valamint amacrin (A) sejteket.
A struktúra szépsége persze nem feledteti a működésében rejlő kontraintuitivitást, hiszen a fotoreceptorok a retina legmélyén fekszenek, így a fotonoknak át kell verekedniük magukat a felettük található további sejttípusokon, na meg a szem belső érhálózatán is (hogy ez miért is alakulhatott így, arról lásd a szemfejlődéses posztot). És mintha ez nem lenne elég, az egyes fotoreceptor" sejtek nem akkor tüzelnek, amikor fény éri őket, hanem épp fordítva: a csapok és pálcikák folyamatosan aktív állapotban vannak, és fény hatására "lefagynak" (ezt hívjuk tudományosabban hiperpolarizációnak), aminek következtében ilyenkor kevesebb ingerületátvivő anyagot bocsátanak ki. Mivel hamarosan igen lényegessé válik, még annyit bonyolítanék a dolgon, hogy a csapsejtek keltette furcsa ingerület- kakofóniából aztán a bipoláris sejtek hámozzák ki a lényeget két alapvető mechanizmus segítségével, ui. a csap-bipoláris sejtek további két nagy osztályba sorolhatók, aszerint, hogy akkor továbbítanak információt, ha a csapsejteket fény éri (ún. ON-bipoláris sejtek), vagy akkor, ha a csapsejtre eső fény intenzitása csökken (OFF-bipoláris sejtek).
Persze kontraintuitivitás ide vagy oda, a rendszer – mint azt a poszt olvasása bizonyítja – egész tűrhetően működik legtöbbünkben, és bármily obskurus is a fotoreceptor-sejtek viselkedése, elvesztésük megvakuláshoz vezet. Az ún. retinális degeneráció sok ezer ember életét keseríti meg, így nem meglepő, hogy sokan igyekeznek ellene valami ellenszert kiagyalni.
Mivel a fotoreceptor-sejtek elpusztulása egyúttal a fényérzékeny opszinmolekulák elvesztését is jelenti, a teljes retina-hálózat lefagy, hiszen a maradék sejtek, bármennyire is egészségesek is, képtelenek lesznek a fotonokat valamilyen sejtszintű kémiai jellé alakítani. Hacsak…. nem segítünk be egy kicsit. És hogy ez nem teljesen elszállt ötlet, azt bizonyítja Roska Botond csoportjának napokban megjelent cikke.
Nem meglepő módon természetesen nem mindegy, hogy a retina melyik másik sejtjét tesszük "fényérzékennyé"; a folyamatosan tüzelő ON- és OFF-bipoláris, illetve amacrin és horizontális sejtek keltette káoszból látókéreg legyen a talpán, amelyik kihámozza a lényeget. Roskáék épp ezért azt használták ki, hogy néhány gén specifikusan csak az ON-bipoláris sejtekben fejeződik ki. Egy ilyen génnek, a Grm6-nak a szabályozó régióját fűzték egy zöldalgákból izolált, fényre aktiválódó ioncsatorna kódoló szekvenciájához, és az így létrehozott DNS szakaszt juttatták retinális degenerációban szenvedő egerek szemébe. Így ha a szemüket fény érte, az ON-bipolárisok (amelyeket normális esetben épp ilyenkor aktivizálna a velük kapcsolatban levő csapsejt) tüzelni kezdtek. A rendszer olyannyira működőképesnek bizonyult, hogy hat hónappal később számos egér még mindig képes volt fényérzékelésre. Ne kristálytiszta, "ötmegapixeles" képre tessék gondolni, inkább csak egyszerű sötétség-világosság megkülönböztetésre. De ez akkor is végtelenszer több információ, mint amit ezeknek az egereknek a retinája egyébként generálna…
(Az egér retinát ábrázoló illusztráció Rachel Wong honlapjáról származik.)
Lagali PS, Balya D, Awatramani GB, Münch TA, Kim DS, wt al. (2008) Light-activated channels targeted to ON bipolar cells restore visual function in retinal degeneration. Nat Neurosci doi:10.1038/nn.2117
