Az organoidok, vagyis miniatűr, in vitro (lásd még “Petri csészében”) létrehozott szövetdarabok kutatása az utóbbi években mindenképpen a leggyorsabban fejlődő biológiai tudományterületet jelenti és manapság már tényleg (hogy elpuffantsuk az idekívánkozó nagy közhelyet) nem múlik el hét 1-2 fajsúlyosabb organoidos publikáció nélkül.
Madártávlatból nézve, két nagy csoport különíthető el organoidok esetében: azok, amelyek nagyon széles differenciációs potenciállal rendelkező “pluripotens” (akár klasszikus, embrionális, akár újgenerációs indukált) őssejtekből jönnek létre és azok, amelyek szűkebb potenciállal rendelkező, “multipotens” őssejtekből alakulnak ki. Utóbbiak döntően a felnőtt, kifejlett egyedek egyes szöveteiben jelen levő őssejtek felhasználásával létrehozott organoidok és ennek a területnek az egyik legfontosabb úttörője a pár éve Breakthrough Prize-al is kitüntetett Hans Celvers.
Clevers csoportja a holland Hubrecht Institute-ban még a 2010-es évek elején ért el komoly áttöréseket a bél-organoidok létrehozásával és kutatásával, azóta pedig, talán csak minimális túlzással, nincs olyan hámszövettel (epitéliummal) borított szerv, amelyből ne készítettek volna organoidokat. Az utóbbi években különböző mirigyekre kezdtek koncentrálni, ehhez kapcsolódott egy tavalyi publikációjuk, ahol például méreg-termelésre képes kígyó méregmirigy-organoidokat csináltak. Most pedig, a jól bejáratott metodológiájukkal a könnymirigyet vették górcső alá.
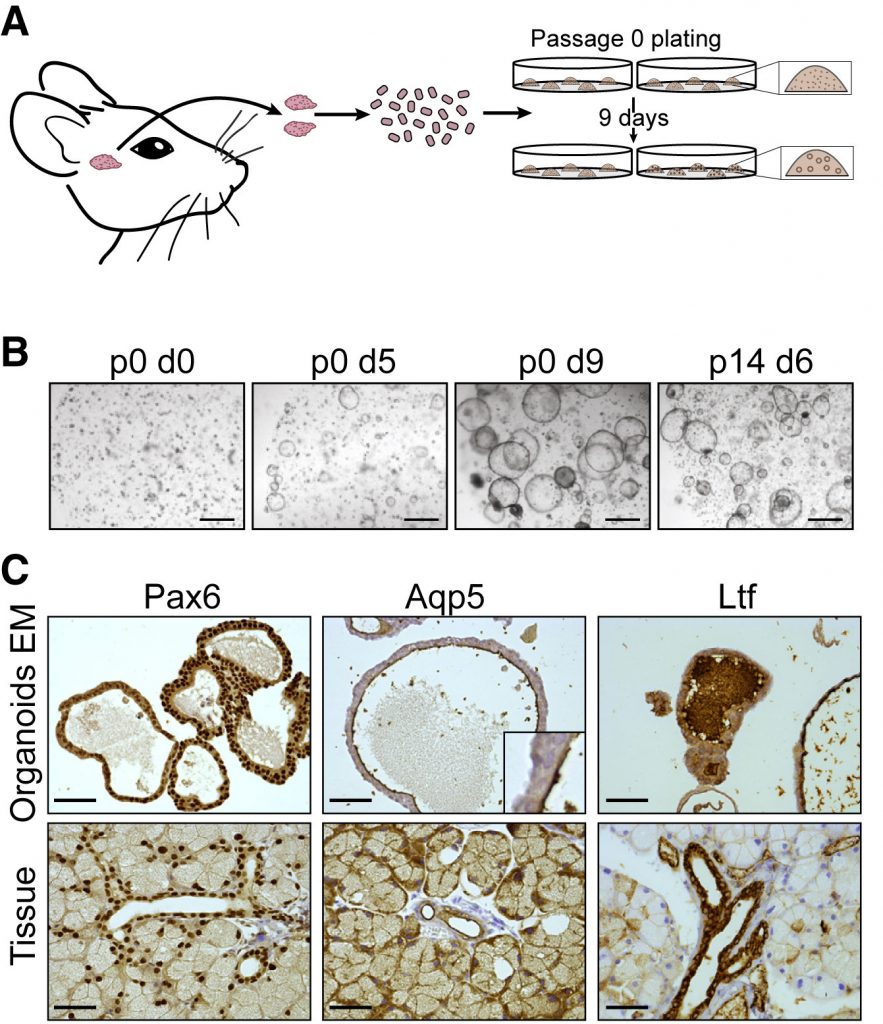
Az ilyen organoid-készítős tanulmányoknak a kezdeti lépései mindig nagyon hasonlóak: a vizsgált szervet szétszedik sejtekre, amelyeket utána egy in vitro közegben próbálnak meg tenyészteni. Ha a sejtek között vannak őssejtek is, akkor a megfelelő közeg kikísérletezése után előbb-utóbb megjelennek a labda alakú organoidok. Most is ez történt, előbb emberi, majd egér könnymirigyből kiindulva hozták létre ezeket az organoidokat (alább csak az egér esetet mutatom), amelyek kb. 10 nap alatt ∼200 μm átmérőjű gömbökké nőtték ki magukat és a szövettenyészetek fenntartására klasszikusan használt “passzálások” (újabb tenyészet indítása a sejtekből) után is megmaradt ez a jelleg (az ábra B paneljén a “pX” azt jelenti, hogy X db. passzálás után; a “0” azt jelenti, hogy a frissen létrehozott szövetet jellemzik.) Az organoidok több olyan fehérjét kifejeztek, ami a könnymirigyre is jellemző, sőt a belsejükben, hasonlóan a valódi könnymirigyek belsejéhez az antimikrobiális hatású Lactotransferrin (Ltf) is megjelenik.
Ha pedig van egy olyan organoid-rendszerünk, amely gyakorlatilag szinte korlátlan mennyiségben (viszonylag olcsón) tudja biztosítani egy valódi szerv miniatűr vázát, hirtelen a lehetőségek elég széles tárháza nyílik meg. Nagyon részletesen lehet vizsgálni a szerv kialakulásának folyamatát, az egyes gének szerepét (ezáltal genetikai-eredetű betegségek kialakulását), vagy azt is, hogy az organoidot visszaültetve, mennyire lesz működőképes (ez potenciális terápia lehet a jövőben pl. Sjögren-szindróma típusú autoimmun betegségekre). Én csak egy aspektust emelnék ki ebből a tanulmányból, mégpedig azt, hogy az organoidok miképp tehetik lehetővé a könnyezést befolyásoló szerek gyors keresését.
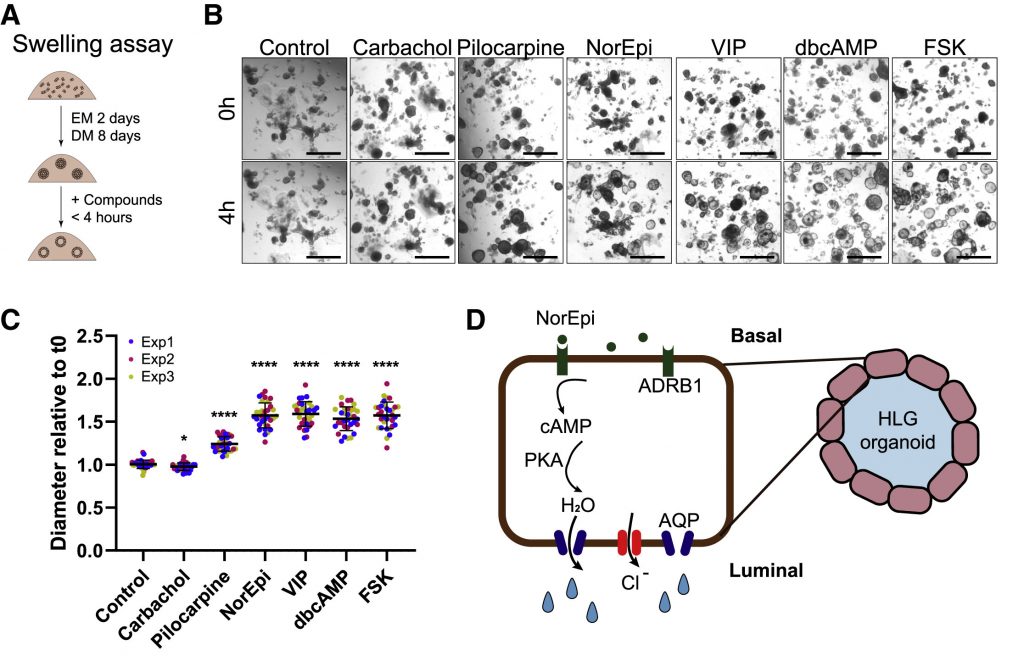
A munka ezen részéhez már emberi könnymirigyből származó organoidokat használtak és lényegében arról van szó, hogy különböző anyagokat tettek az organoidok közegéhez. Normális könnymirigynél a könny az elvezetődik, de az organoid egy zárt rendszer, így a megtermelődő, az organoid belsejébe ürülő könny lufiként “felfújja” az organoidokat. Ezt a méretváltozást pedig elég könnyen lehet automatizálva is detektálni, s ahogy az a fenti ábrán is látható, elég gyorsan lehet szűrni azokat az anyagokat, amelyek könnyezést tudnak indukálni.
Miért lehet ez hasonló, miért akarnák elérni, hogy valaki könnyezzen (és miért nem hámoztatunk vele hagymát)? A helyzet az, hogy bár egy könnymirigy anatómiailag elég egyszerű rendszer, még nem értjük teljesen, miképp működik. Ha pedig olyan anyagokkal, amelyeket korábban már pontosan jellemeztek (tudjuk pl. milyen molekulákhoz kapcsolódnak és befolyásolnak) sikerül befolyásolnunk, közelebb kerülhetünk ahhoz, hogy megértsük, a valóságban hogyan történhet a könnymirigy működésének szabályozása.
(A borítókép a Pixabay-ről származik.)
Korving J, Trani Bustos M, Gehart H, Begthel H, Bar-Ephraim YE, et al. (2021) Exploring the human lacrimal gland using organoids and single-cell sequencing. Cell Stem Cell doi: 10.1016/j.stem.2021.02.024.
